Презентация "Вещество и энергия" (8 класс) по химии – проект, доклад
Презентацию на тему "Вещество и энергия" (8 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 18 слайд(ов).
Слайды презентации
Список похожих презентаций
Вещество вода
Любая ли вода полезна? Работа в группах Вода! Вода? Вода… (группа теоретиков) Вода - источник жизни (группа экологов) Где искать воду? (группа историков ...Вещество
Человек связан с окружающим его миром живой и неживой природы тысячами незримых нитей. Он и сам является ее частью. Природа кормит, поит человека, ...Вещество в химии
Сегодня мы начинаем изучать одну из самых древних из важных наук- химию. А что же изучает химия? Химия – это наука о веществах, их свойствах и превращениях. ...Вещество
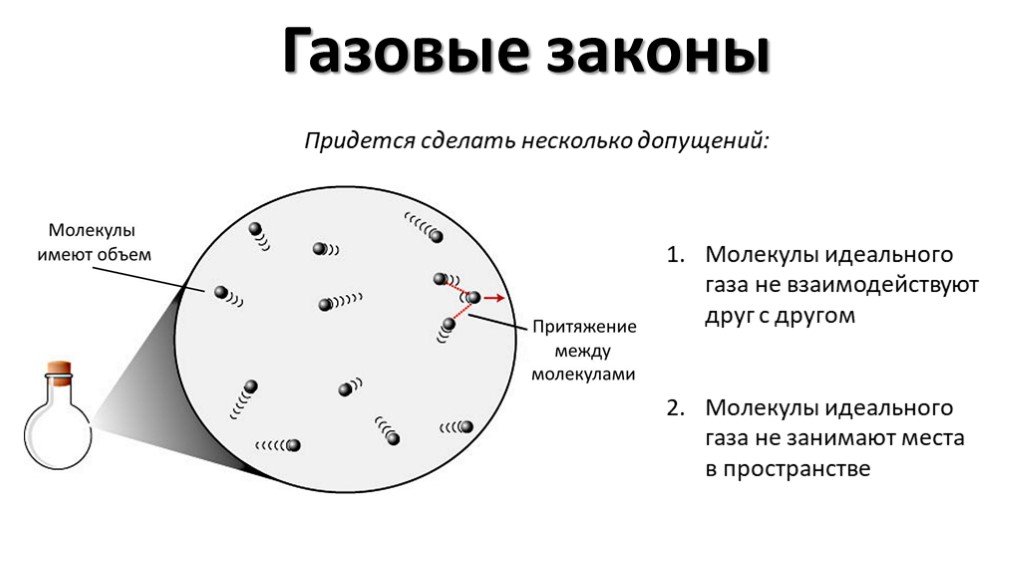
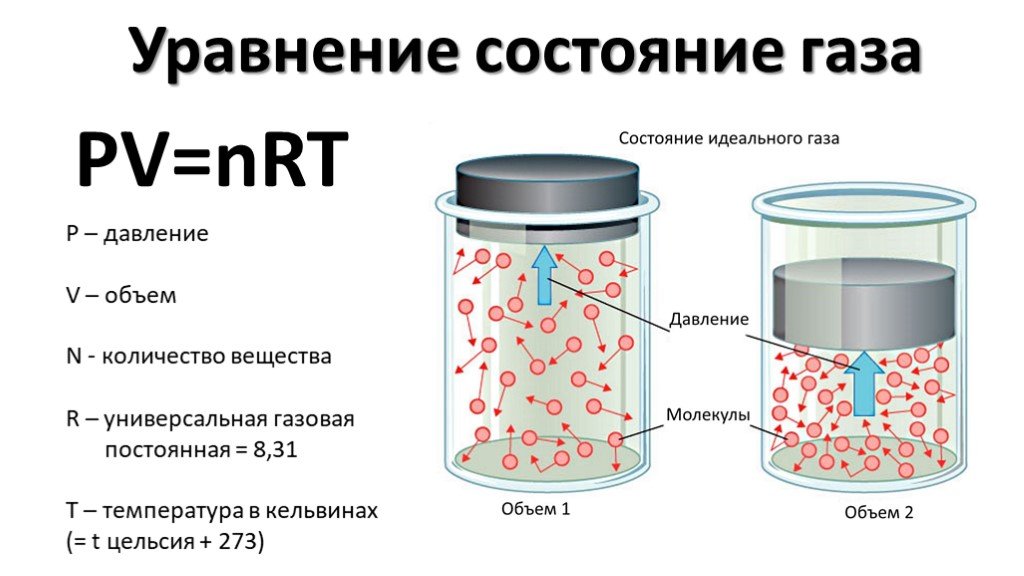
Химия это наука о веществах, их свойствах и превращениях их друг в друга. С какими науками связана химия? Что такое тела? Что такое вещество? Тела ...Газовые законы
План изучения изопроцесса в газе. Дать определение процесса. Записать уравнение состояния газа для данного процесса, связывающее изменяющиеся параметры. ...Углеводы химия
Содержание. Классификация углеводов Моносахариды Нахождение в природе Изомерия Получение Физические свойства Химические свойства Источники информации. ...Происхождение нефти и газа
Происхождение нефти и газа до настоящего времени не выяснено . Существует множество теорий происхождения нефти и газа, каждая их которых имеет подтверждение ...Современная химия
Учение о составе вещества. Химический элемент - вид атомов с одинаковым зарядом ядра. Индивидуальность химического элемента обусловлена: зарядом ядра ...Органическая химия
ФЕНОЛЫ. 2. Классификация и изомерия Как и спирты, фенолы бывают одноатомные (одна -OH) и многоатомными (несколько -OH). Для фенолов характерна изомерия ...«Нуклеиновые кислоты» химия
Цель урока: сформировать у студентов понимание взаимосвязанности и взаимозависимости веществ в клетке. Задачи урока: повторить строение и основные ...Кто ты и откуда химия?
Откуда пошло слов химия? Хи́мия (от араб. کيمياء, предположительно от египетского «chemi» — чёрный, откуда также греческое название Египта, чернозёма ...Молекулярно - кинетическая теория идеального газа
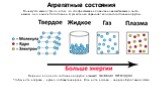
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ. ВСЕ ТЕЛА СОСТОЯТ ИЗ МОЛЕКУЛ. МОЛЕКУЛЫ НАХОДЯТСЯ В БЕСПРЕРЫВНОМ ДВИЖЕНИИ. МЕЖДУ МОЛЕКУЛАМИ СУЩЕСТВУЮТ СИЛЫ ВЗАИМОДЕЙСТВИЯ. ...Агрегатное состояние вещества
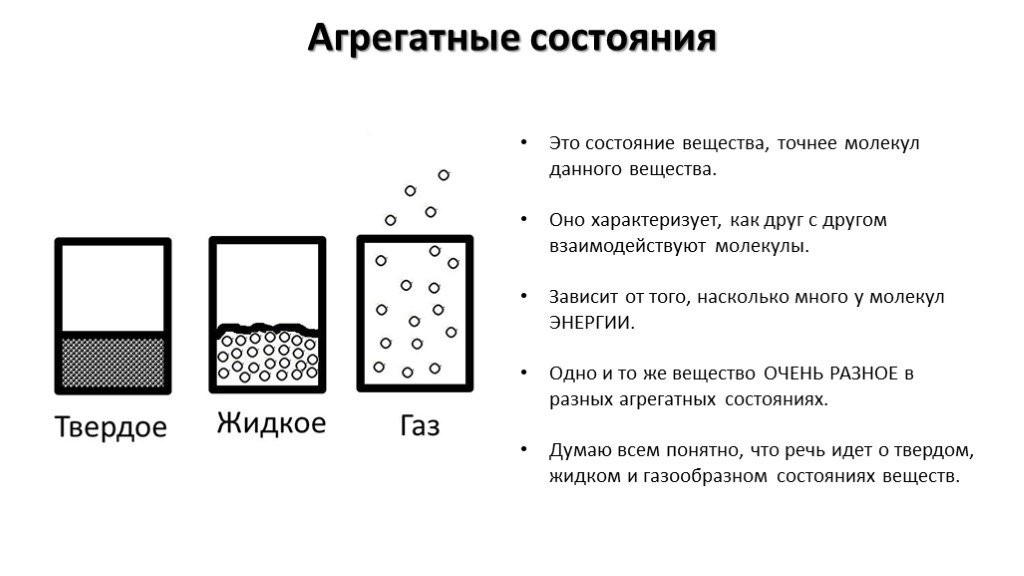
Существуют 3 основных агрегатных состояния вещества. Газообразное Твердое Жидкое. Чем же различаются данные вещества. Агрегатное состояние. Различия. ...Агрегатное состояние вещества
Твердое тело. Состояние, характеризующееся способностью сохранять объём и форму. Атомы твёрдого тела совершают лишь небольшие колебания вокруг состояния ...Агрегатное состояние вещества
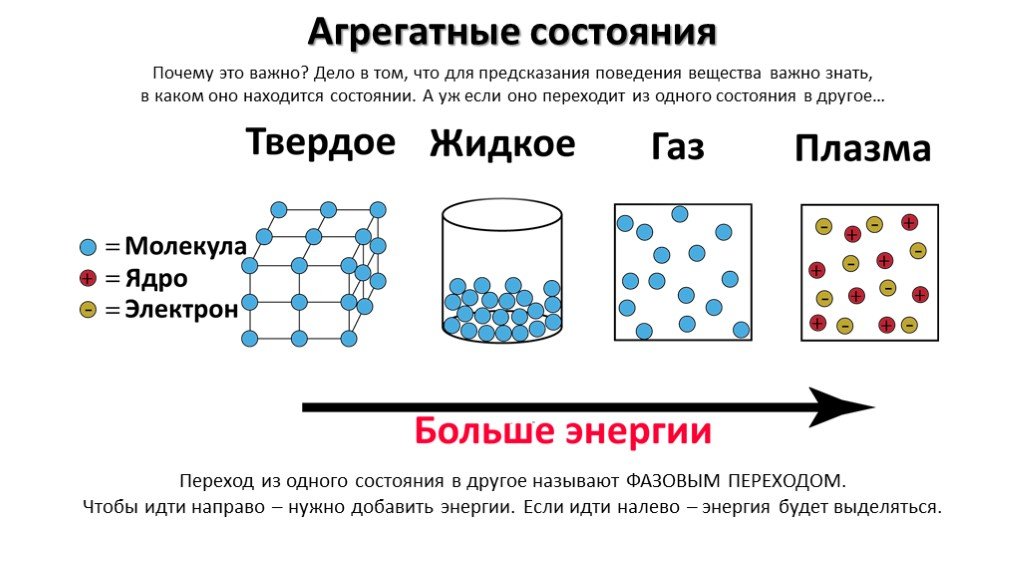
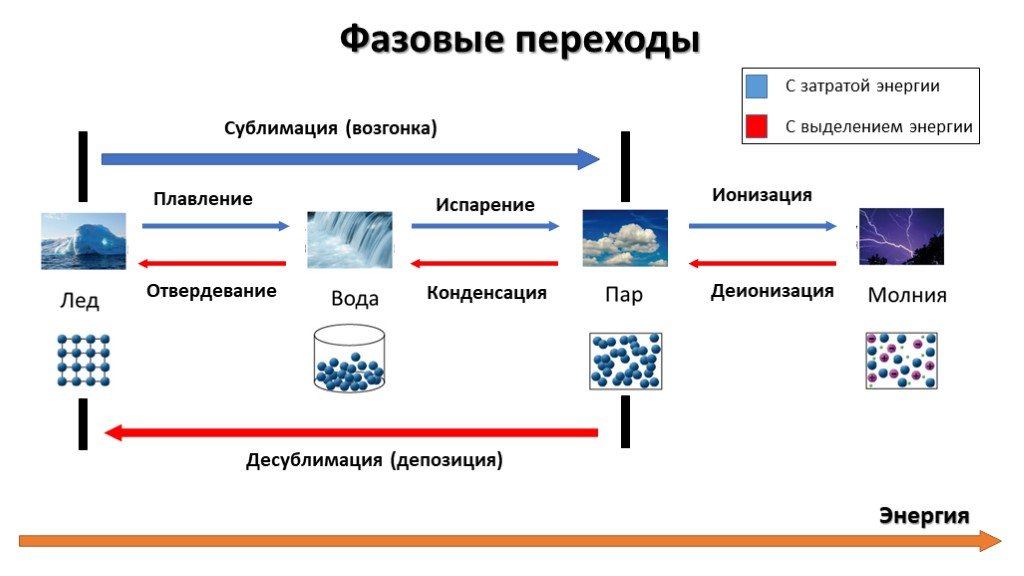
Три состояния вещества. Газ Жидкость Твердое тело. Твердое. Жидкое. Газообразное состояние. Процессы с поглощением и выделением тепла. Плавление Парообразование ...Агрегатное состояние вещества
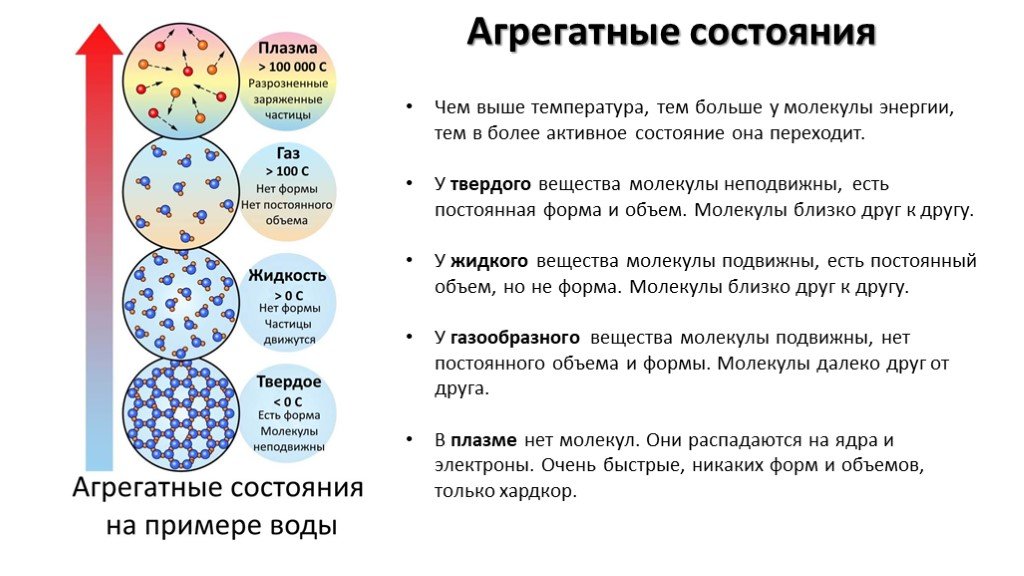
Общие понятия. Агрегатное состояние вещества- состояние вещества, характеризующееся определенными качественными свойствами. Строение твердых тел. ...Агрегатное состояние
агрегатное состояние вещества. О том, что лед может превращаться в воду, а вода - в пар, было известно с незапамятных времен. Однако то, что лед, ...«Электролитическая диссоциация» химия
Электролитическая диссоциация. H2O. Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией. ...«Окислительно-восстановительные реакции» химия
СОДЕРЖАНИЕ:. 1. Какие реакции называются окислительно-восстановительными? 2. Что называют окислителем, восстановителем? 3. Окислительно-восстановительный ...Кислотно-щелочное состояние
Кислотно-щелочное состояние (КЩС) рассматривают как совокупность физико-химических, биологических, биохимических и других процессов, поддерживающих ...Конспекты
Предмет химии. Вещество
Предмет химии. Вещество. Цели урока:. Обучающая:. сформировать представление о предмете химии. Дать первоначальные понятия о веществе, химическом ...Предмет химии. Вещество
Разработка урока в 8-м классе "Предмет химии. Вещество". Цели урока:. Обучающая:. сформировать представление о предмете химии. Дать первоначальные ...Вещество Х
Открытый урок. Углеводы. «Вещество Х». Данный открытый урок проводится по программе в 10 классе с базовым изучением ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:15 февраля 2019
Категория:Химия
Содержит:18 слайд(ов)
Поделись с друзьями:
Скачать презентацию