Презентация "Железо и его свойства" по химии – проект, доклад
Презентацию на тему "Железо и его свойства" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 13 слайд(ов).
Слайды презентации
Список похожих презентаций
Железо, его соединения и их свойства
Задачи:. Проверить знание основных теоретических вопросов темы “Железо и его соединения”; Развивать умения составлять электронный баланс и уравнения, ...Азот и его свойства
История открытия азота:. В 1772 г. Англичанин Д. Резерфорд установил, что воздух, оставшийся под колоколом, где жила несколько дней мышь, освобожденный ...Кислород. Получение кислорода и его физические свойства
Цель. сформировать понятия кислород как атом и молекула; изучить физические и химические свойства кислорода, нахождение его в природе; рассмотреть ...Углерод и его свойства
Строение атома. В периодической таблице химических элементов углерод (С) расположен во втором периоде, в IV группе главной подгруппы. Углерод (С) ...Фенол и его свойства
Задачи урока. Изучить состав, строение фенола и его соединений. Рассмотреть зависимость взаимного влияния атомов в молекуле фенола на его свойства. ...Крахмал и его свойства
Крахма́л (C6H10O5)n — полисахариды амилозы и амилопектина, мономером которых является альфа-глюкоза. Крахмал, синтезируемый разными растениями в хлоропластах, ...Углерод и его свойства
Строение атома углерода. Углерод (лат. Carboneum) С – химический элемент IV группы периодической системы Менделеева: атомный номер 6, атомная масса ...Строение атома и его свойства
Атом какого химического элемента имеет приведенную ниже схему строения? 1) аргона 2) кислорода 3) серы 4) кальция. . Сколько электронов находится ...Железо и его соединения
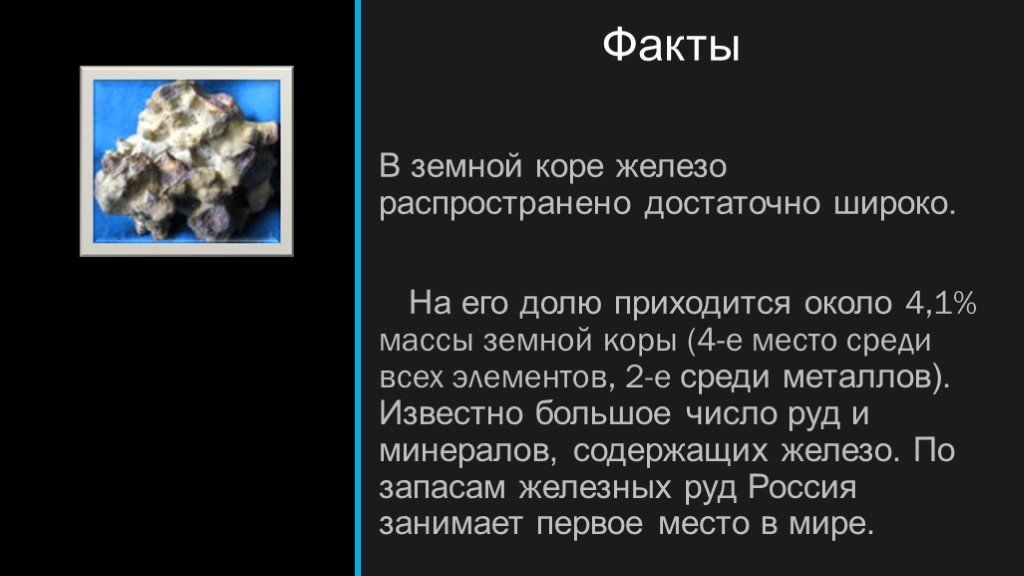
Желе́зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером ...Каучук и его свойства
Цель:. Ознакомление учащихся со свойствами натурального каучука его составом и строением, вулканизацией. План:. 1. История открытия каучука. 2. Натуральные ...Железо и его соединения
Закрепление и обобщение материала по теме: «Железо и его соединения». 9 класс. Путешествие по стране химических вопросов. ЗНАНИЯ - ЭТО ИСТИННЫЕ СОКРОВИЩА, ...Железо и его соединения
С О Д Е Р Ж А Н И Е. Положение В периодической системе. НАХОЖДЕНИЕ В ПРИРОДЕ. ОТКРЫТИЕ И ПОЛУЧЕНИЕ. ХИМИЧЕСКИЕ СВОЙСТВА. ЖЕЛЕЗО В ОРГАНИЗМЕ И ЕГО ...Алюминий и его свойства
Алюминий и его свойства. ППС. Химическая активность. Взаимодействие с простыми веществами. Взаимодействие с сложными веществами. получение лабораторное ...Метан и его свойства
Предельные углеводороды. Метан. Алканы. Общая формула предельных углеводородов. CnH2n+2 где n≥1. При образовании связей атома углерода с водородом ...Железо и его соединения
Загадка Очень древний я металл, Счёт столетьям потерял. Был нескромным я не в меру, Тысячи лет до нашей эры. А за блеск, мерцавший холодом, Люди там ...Графит и его свойства
Графи́т -минерал из класса самородных элементов, одна из аллотропных видоизменений углерода. Структура слоистая. Слои слабоволнистые, почти плоские, ...Его Величество Железо
ЦЕЛИ:. Ознакомиться с особенностями металлургического комплекса России Изучить химические и физические свойства простого вещества - железа, ознакомиться ...Алюминий, его Свойства и применение
Al 13. Алюминий (лат. Aluminium). 3 8 2 26,9815 3s2 3p1. Был впервые получен датским физиком Х.К. Эрстедом в 1825 г. Название этого элемента происходит ...Бензол и его свойства
История открытия бензола Второе рождение Новое получение Строение бензола Схема перекрывания облаков в молекуле Физические свойства Химические свойства ...Водород, его общая характеристика, нахождение в природе и его свойства
Цели. сформировать знания учащихся о водороде как о атоме и простом веществе, его способах получении, свойствах и применении научить учащихся работать ...Конспекты
Железо, ЕГО СТРОЕНИЕ, СВОЙСТВА И ПРИМЕНЕНИЕ
Государственное бюджетное общеобразовательное учреждение. Центр образования №80. Центрального района города Санкт-Петербурга. Методическое объединение ...Железо. Положение железа в периодической системе и строение его атома. Нахождение в природе. Физические и химические свойства железа
Дата_____________ Класс_______________. Тема:. Железо. Положение железа в периодической системе и строение его атома. Нахождение в природе. Физические ...Кислород, его общая характеристика. Нахождение в природе.Получение и свойства кислорода
Урок химии в 8 классе «Кислород, его общая характеристика. Нахождение в природе.Получение и свойства кислорода». Цель: . изучение и первичное осознание ...Фосфор и его свойства
Государственное казенное общеобразовательное учреждение Ростовской области. общеобразовательная школа-интернат основного общего образования. п. ...Железо и его соединения
Железо и его соединения. МБУ лицей № 51 г.о.Тольятти. . 9 класс. . Тип урока:. урок формирования новых знаний и умений с использованием групповых ...Железо и его соединения
Тема:. Задачи:. Образовательные:. Воспитательные:. Развивающие:. Тип урока:. Методы и методические приёмы:. Оборудование:. ...Железо и его соединения
Начальное профессиональное образование. Профессиональное училище №63. Г. Гуково Ростовской области. Конспект урока по химии. . 9 класс. ...Железо и его соединения
ТЕМА: «Железо и его соединения». . Цель:. . . Изучить физические свойства железа. Охарактеризовать место. Fe. в П.С.Х.Э. изучить химические ...Водород. Его получение и свойства
Маркелова Светлана Алексеевна. . План-конспект открытого урока. . по химии. 9-го класса. на тему. Водород. Его получение и свойства. ...Водород. Его получение и свойства
План-конспект открытого урока. . по химии для. 9-го класса. на тему:. «Водород. Его получение и свойства». Тема урока:. Водород. Его получение ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:10 января 2019
Категория:Химия
Содержит:13 слайд(ов)
Поделись с друзьями:
Скачать презентацию