Слайд 1Химия Для I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конструирование изделий и материалы легкой промышленности ИИИБС, кафедра ЭПП к.х.н., доцент А. Н. Саверченко
Слайд 2Биополимеры
[Подзаголовок] (24 pt)
Слайд 3Студент должен: знать названия, стоение и свойства биополимерах Уметь Составлять формулы и описывать свойства биополимеров
Слайд 4Биополиме́ры — класс полимеров, встречающихся в природе в естественном виде, входящие в состав живых организмов: белки, нуклеиновые кислоты, полисахариды. Биополимеры состоят из одинаковых (или разных) звеньев — мономеров. Мономеры белков — аминокислоты, нуклеиновых кислот — нуклеотиды, в полисахаридах — моносахариды.
Кристаллы различных белков, выращенные на космической станции «Мир» и во время полётов шаттлов НАСА. Высокоочищенные белки при низкой температуре образуют кристаллы, которые используют для получения модели данного белка.

Слайд 5Мономе́р (с греч. mono "один" и meros "часть") — это небольшая молекула, которая может образовать химическую связь с другими мономерами и составить полимер.Стоит отметить, что другие низкомолекулярные вещества принято называть димерами, тримерами, тетрамерами, пентамерами и т.д., если они, соответственно, состоят из 2, 3, 4, и 5-ти мономеров.
Приставку олиго- (сахариды, меры, пептиды) добавляют в общем случае, когда полимер состоит из небольшого количества мономеров. Мономеры могут быть как органическими, так и неорганическими.
Слайд 6Примерами органических мономеров могут служить молекулы углеводородов, такие, как алкены и арены. К примеру, полимеризация этена приводит к образованию такой широко известной пластмассы, как полиэтилен. Липиды также являются составленными из мономеров жирных кислот и глицерина. Также в промышленности широко используют акриловые мономеры — акриловую кислоту, акриламид.
Слайд 7В результате полимеризации природных мономеров — аминокислот, образуются белки. Мономеры глюкозы образуют различные полисахариды — гликоген, крахмал. Выделяют два типа биополимеров — регулярные (некоторые полисахариды) и нерегулярные (белки, нуклеиновые кислоты, некоторые полисахариды).
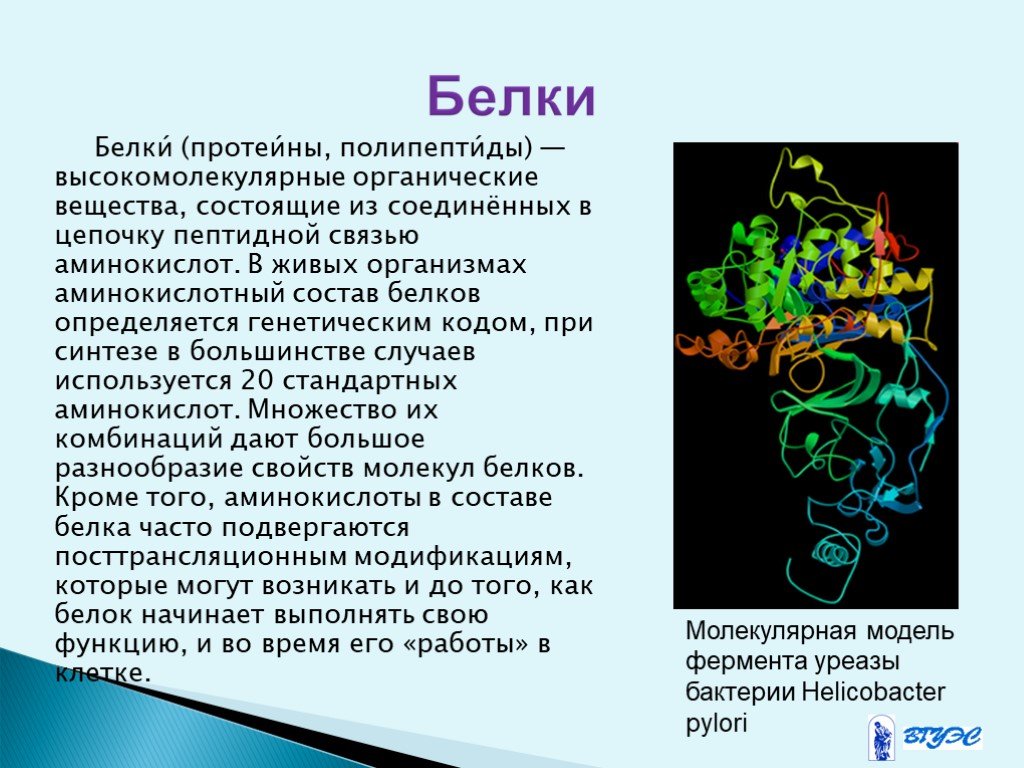
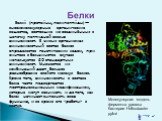
Слайд 8Белки́ (протеи́ны, полипепти́ды) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью аминокислот. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций дают большое разнообразие свойств молекул белков. Кроме того, аминокислоты в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его «работы» в клетке.
Молекулярная модель фермента уреазы бактерии Helicobacter pylori

Слайд 9Кроме последовательности аминокислот полипептида (первичной структуры), крайне важна трёхмерная структура белка, которая формируется в процессе сворачивания (фолдинга (от англ. folding), то есть сворачивание). Трёхмерная структура формируется в результате взаимодействия структур более низких уровней. Выделяют четыре уровня структуры белка. Уровни структуры белков: 1 — первичная, 2 — вторичная, 3 — третичная, 4 — четвертичная

Слайд 10Гибкость макромолекул — это их способность обратимо (без разрыва химических связей) изменять свою форму. Особенности полимеров, обусловленные гибкостью макромолекул, проявляются при деформировании полимеров. В отсутствие внешних воздействий равновесным состоянием гибкой макромолекулы является форма рыхлого клубка (максимум энтропии). При деформации полимера макромолекулы распрямляются, а после снятия деформирующей нагрузки, стремясь к равновесному состоянию, они снова сворачиваются за счет поворотов вокруг σ- связей в результате теплового движения. Это является причиной высоких обратимых деформаций (эластичности) полимеров.
Слайд 11Это последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, важных для функции белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним можно предсказать функцию неизвестного белка.
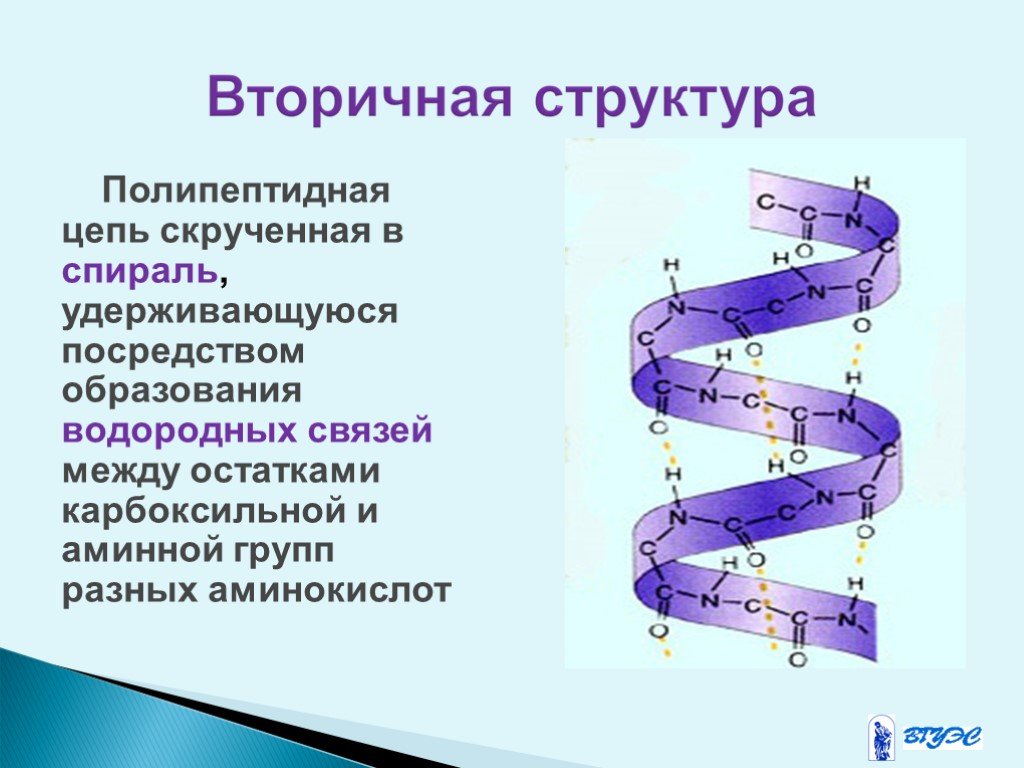
Слайд 12Полипептидная цепь скрученная в спираль, удерживающуюся посредством образования водородных связей между остатками карбоксильной и аминной групп разных аминокислот
Слайд 13пространственное строение полипептидной цепи — взаимное расположение элементов вторичной структуры, стабилизированное взаимодействием между боковыми цепями аминокислотных остатков. В стабилизации третичной структуры принимают участие: ковалентные связи (между двумя цистеинами — дисульфидные мостики); ионные (электростатические) взаимодействия (между противоположно заряженными аминокислотными остатками); гидрофобные взаимодействия. водородные связи;
Слайд 14Объединение в единую структуру нескольких молекул с третичной организацией (гемоглобин, инсулин)
Слайд 15Водородная связь — разновидность невалентного взаимодействия между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR'. Результатом таких взаимодействий являются комплексы RA-H•••BR различной степени стабильности, в которых атом водорода выступает в роли мостика, связывающего фрагменты RA и BR.
Слайд 16Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 КДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 КДж/моль для ион-молекулярных комплексов (AHB)±; так, для комплекса (H2O•H•OH2)+ образованного H2O и H3O+ - 132 КДж/моль в газовой фазе.
Слайд 17Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. В частности, элементы вторичной структуры (например, α-спирали, β-складки) в молекулах белков стабилизированы водородными связями. Водородные связи во многом обуславливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты,амиды карбоновых кислот, сложные эфиры).
Слайд 18Белки имеют несколько уровней организации — первичная, вторичная, третичная, и иногда четвертичная. Первичная структура определяется последовательностью мономеров, вторичная задаётся внутри- и межмолекулярными взаимодействиями между мономерами, обычно при помощи водородных связей. Третичная структура зависит от взаимодействия вторичных структур, четвертичная, как правило, образуется при обьединении нескольких молекул с третичной структурой.
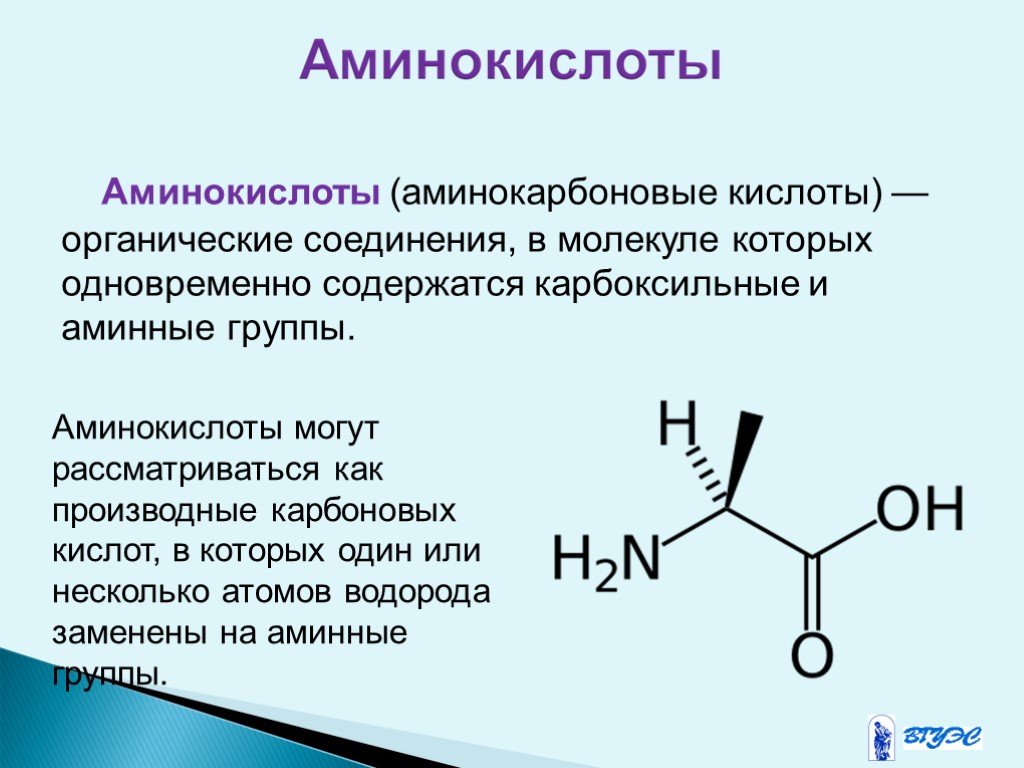
Слайд 19Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.

Слайд 201. Аминокислоты могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы -COOH, так и основные свойства, обусловленные аминогруппой -NH2. Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов. 2. Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков и нейлона-66. 3. Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов. 4. Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.

Слайд 21В процессе биосинтеза белка в полипептидную цепь включаются 20 важнейших α-аминокислот, кодируемых генетическим кодом. Часто для запоминания однобуквенного обозначения используется мнемоническое правило.
Аланин Аргинин Аспарагиновая кислота Аспарагин Валин Гистидин Глицин Глутаминовая кислота Глутамин Изолейцин
Лейцин Лизин Метионин Пролин Серин Тирозин Треонин Триптофан Фенилаланин Цистеин
Слайд 22Аланин — алифатическая аминокислота. Химическая формула HO2CCH(NH2)CH3 α-Аланин входит в состав многих белков, β-аланин — в состав ряда биологически активных соединений. Аланин легко превращается в печени в глюкозу и наоборот. Этот процесс носит название глюкозо-аланинового цикла и является одним из основных путей глюконеогенеза в печени.
Слайд 23Аланин, сеаминопропионовая кислота, ациклическая аминокислота, широко распространённая в живой природе. Является важным источником энергии для мышечных тканей, головного мозга и центральной нервной системы; укрепляет иммунную систему путем выработки антител; активно участвует в метаболизме сахаров и органических кислот. Помимо этих аминокислот, называемых стандартными, в некоторых белках присутствуют специфические нестандартные аминокислоты, являющиеся производными стандартных. В последнее время к стандартным аминокислотам иногда причисляют селеноцистеин (Sec, U).
Слайд 24По R-группам Неполярные: аланин, валин, изолейцин, лейцин, метионин, пролин, триптофан, фенилаланин Полярные незаряженные (заряды скомпенсированы)при pH=7: аспарагин, глицин, глутамин, серин, тирозин, треонин, цистеин Полярные заряженные отрицательно при pH=7: аспарагиновая кислота, глутаминовая кислота Полярные заряженные положительно при pH=7: аргинин, гистидин, лизин

Слайд 25По функциональным группам Алифатические Моноаминомонокарбоновые: аланин, валин, глицин, изолейцин, лейцин Оксимоноаминокарбоновые: серин, треонин Моноаминодикарбоновые: аспарагиновая кислота, глутаминовая кислота, за счёт второй карбоксильной группы имеют несут в растворе отрицательный заряд Амиды Моноаминодикарбоновых: аспарагин, глутамин Диаминомонокарбоновые: аргинин, гистидин, лизин, несут в растворе положительный заряд Серосодержащие: цистеин (цистин), метионин Ароматические: фенилаланин, тирозин Гетероциклические: триптофан, гистидин, пролин (также входит в группу иминокислот) Иминокислоты: пролин (также входит в группу гетероциклических)

Слайд 26Полисахариды, синтезируемые живыми организмами, состоят из большого количества моносахаридов, соединённых гликозидными связями. Зачастую полисахариды нерастворимы в воде. Обычно это очень большие, разветвлённые молекулы. Примерами полисахаридов, которые синтезируют живые организмы, являются запасные вещества крахмал и гликоген, а также структурные полисахариды — целлюлоза и хитин. Так как биологические полисахариды состоят из молекул разной длины, понятия вторичной и третичной структуры к полисахаридам не применяются.
Слайд 27моносахарид H H H H H O глюкоза C6H12O6 H -C – C – C – C – C - C OH OH OH OH OH H
дисахарид C6H12O6 глюкоза сахароза C12H22O11 C6H12O6 фруктоза
полисахарид крахмал (C6H10O5)n
Слайд 28Качественные реакции на глюкозу Реакция серебряного зеркала t C6H12O6 + Ag2O C6H12O7 + 2Ag выделяется серебро Взаимодействие с гидроксидом меди при нагревании t C6H12O6+2Cu(OH)2C6H12O7+Cu2O+2H2O красное окрашивание
Слайд 29Гидролиз сахарозы t0 C12H22O11 + H2O C6H12O6 + C6H12O6 глюкоза фруктоза
Карамелизация t0 C12H22O11темноокрашенные продукты карамелен, карамелин, карамелан
Слайд 30Клейстеризация – с H2O при tо набухание и затем клейстер
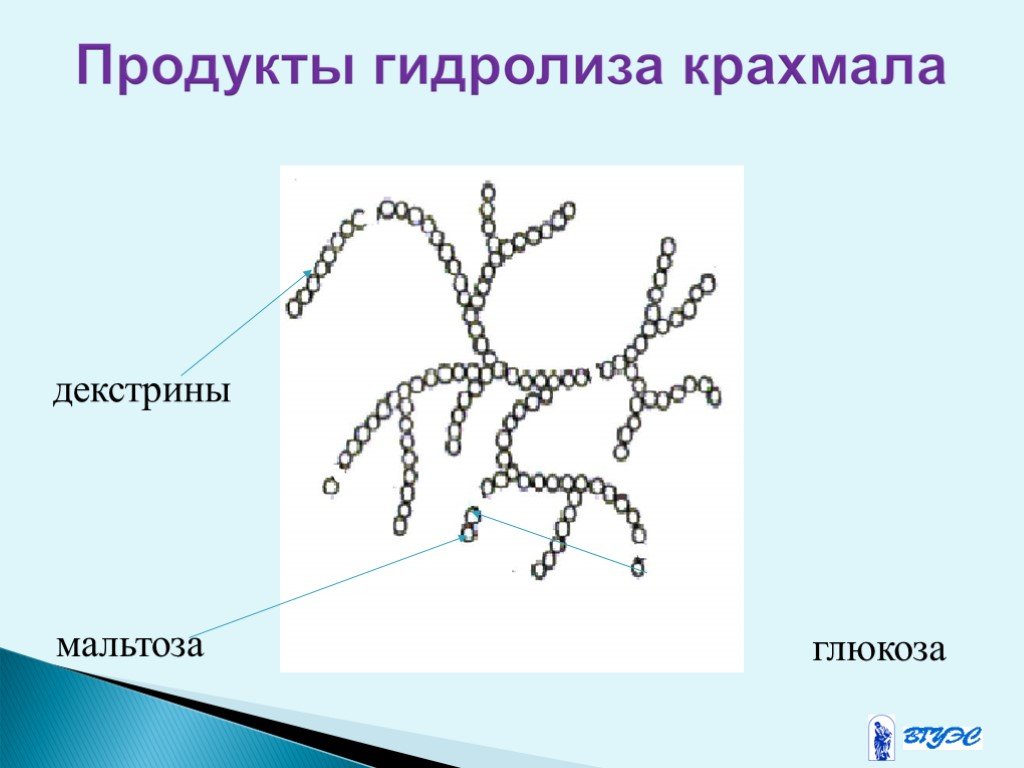
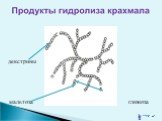
Гидролиз крахмала (C6H10O5)n+ nH2O n C6H12O6 Кислотный гидролиз – при нагревании с H2SO4 образуется глюкоза Ферментативный – под действием ферментов образуются декстрины, а затем – мальтоза и конечный продукт глюкоза
Слайд 31декстрины мальтоза глюкоза
Слайд 32Целлюлоза в форме полимера β-D-глюкозы(иллюстрация) Целлюло́за (от лат. cellula — клетка, то же самое, что клетчатка) — [С6Н7О2(OH)3]n, полисахарид; главная составная часть клеточных оболочек растений. Целлюлоза состоит из остатков молекул глюкозы, которая и образуется при кислотном гидролизе целлюлозы: (C6H10O5)n + nH2O -> nC6H12O6
Слайд 33Серная кислота и йод, благодаря гидролизу, окрашивают целлюлозу в синий цвет. Один же йод — только в коричневый. Кроме целлюлозы, в состав клеточных оболочек входят еще несколько других углеводов, известных под общим именем гемицеллюлоз, извлекаемых из клеточных оболочек 1%-м раствором соляной или серной кислоты при нагревании. С возрастом многие клеточные оболочки перестают давать реакцию на целлюлозу, потому что одни подвергаются одревеснению, другие — опробковению и т. д.
Слайд 34Почти чистой клетчаткой является хлопок, который идет на изготовление ткани. Целлюлоза древесины дает бумагу. Целлюлозу и ее эфиры используют для получения искусственного волокна (вискозный, ацетатный, медно-аммиачный шёлк, искусственная шерсть), пластмасс, кино и фотоплёнок, лаков, бездымного пороха и т. д. Целлюлоза - стойкое вещество,не разрушается при нагревании до 200 C. Не растворима в воде и слабых кислотах. Обладает прочностью, но эластична. Зарегистрирована в качестве пищевой добавки E460.

Слайд 35Рекомендуемая литература
Коровин Николай Васильевич. Общая химия: Учебник. - 2-е изд., испр. и доп. - М.: Высш. шк., 2000. - 558с.: ил. Павлов Н.Н. Общая и неорганическая химия: Учеб. для вузов. – 2-е изд., перераб. и доп. – М.: Дрофа, 2002. – 448 с.: ил. Ахметов Наиль Сибгатович. Общая и неорганическая химия: Учебник для студ. химико-технологических спец. вузов / Н.С.Ахметов. - 4-е изд., исп. - М.:Высш. шк.: Академия, 2001. - 743с.: ил. Глинка Николай Леонидович. Общая химия: Учебное пособие для вузов / Н.Л.Глинка; Ермаков Л.И (ред.) – 29–е изд.; исп. – М.: Интеграл Пресс, 2002 – 727с.: ил. Писаренко А.П., Хавин З.Я. Курс органической химии – М.: Высшая школа,1975,1985. Альбицкая В.М., Серкова В.И. Задачи и упражнения по органической химии. – М.: Высш. шк., 1983. Грандберг И.И. Органическая химия – М.: Дрофа, 2001. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия М.: Высш. Шк., 1981 Иванов В.Г., Гева О.Н., Гаверова Ю.Г. Практикум по органической химии – М.: Академия., 2000.
































![Биополимеры. [Подзаголовок] (24 pt) Биополимеры. [Подзаголовок] (24 pt)](https://prezentacii.org/upload/cloud/18/10/80601/images/thumbs/screen2.jpg)



























![Целлюлоза в форме полимера β-D-глюкозы(иллюстрация) Целлюло́за (от лат. cellula — клетка, то же самое, что клетчатка) — [С6Н7О2(OH)3]n, полисахарид; главная составная часть клеточных оболочек растений. Целлюлоза состоит из остатков молекул глюкозы, которая и образуется при кислотном гидролизе целлю Целлюлоза в форме полимера β-D-глюкозы(иллюстрация) Целлюло́за (от лат. cellula — клетка, то же самое, что клетчатка) — [С6Н7О2(OH)3]n, полисахарид; главная составная часть клеточных оболочек растений. Целлюлоза состоит из остатков молекул глюкозы, которая и образуется при кислотном гидролизе целлю](https://prezentacii.org/upload/cloud/18/10/80601/images/thumbs/screen32.jpg)