Презентация "Аллотропия кислорода" (9 класс) по химии – проект, доклад
Презентацию на тему "Аллотропия кислорода" (9 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 18 слайд(ов).
Слайды презентации
Список похожих презентаций
Применение кислорода
КИСЛОРОД. Кислород - 16-й элемент главной подгруппы VI группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным ...Подгруппа кислорода
Реактивы: сульфат натрия, сульфат меди (ll), лакмус, фенолфталеин, хлорид бария, гидроксид калия, серная кислота Оборудование: набор пробирок (ПХ-14, ...Получение и химические свойства кислорода
Цели и задачи урока:. Выяснить источник кислорода в природе; познакомиться с лабораторными и промышленными способами получения кислорода Познакомиться ...Круговорот кислорода в природе
Круговорот веществ – многократно повторяющийся процесс совместного, взаимосвязанного превращения и перемещения веществ в природе, имеющий более или ...Общая характеристика элементов подгруппы кислорода
ПАМЯТКА К ИЗУЧЕНИЮ ПОДГРУППЫ ЭЛЕМЕНТОВ. 1.Пользуясь Периодической системой, выпишите символы и названия химических элементов, относящихся к данной ...Круговорот кислорода
Цель работы: Уяснить функцию живого вещества на планете, рассмотреть как осуществляется круговорот кислорода в природе. Выяснить источники кислорода ...Кислород. Получение кислорода и его физические свойства
Цель. сформировать понятия кислород как атом и молекула; изучить физические и химические свойства кислорода, нахождение его в природе; рассмотреть ...Задачи Подгруппа кислорода
Практическая работа№2 Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: опытным путем определить растворы следующих веществ: H2SO4 ...Применение кислорода
Кислород необходим практически всем живым существам. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью ...Применение кислорода
Корнелиус Дреббель. Интересным фактом является то, что впервые кислород выделили не химики. Это сделал изобретатель подводной лодки К. Дреббель в ...Горение кислорода
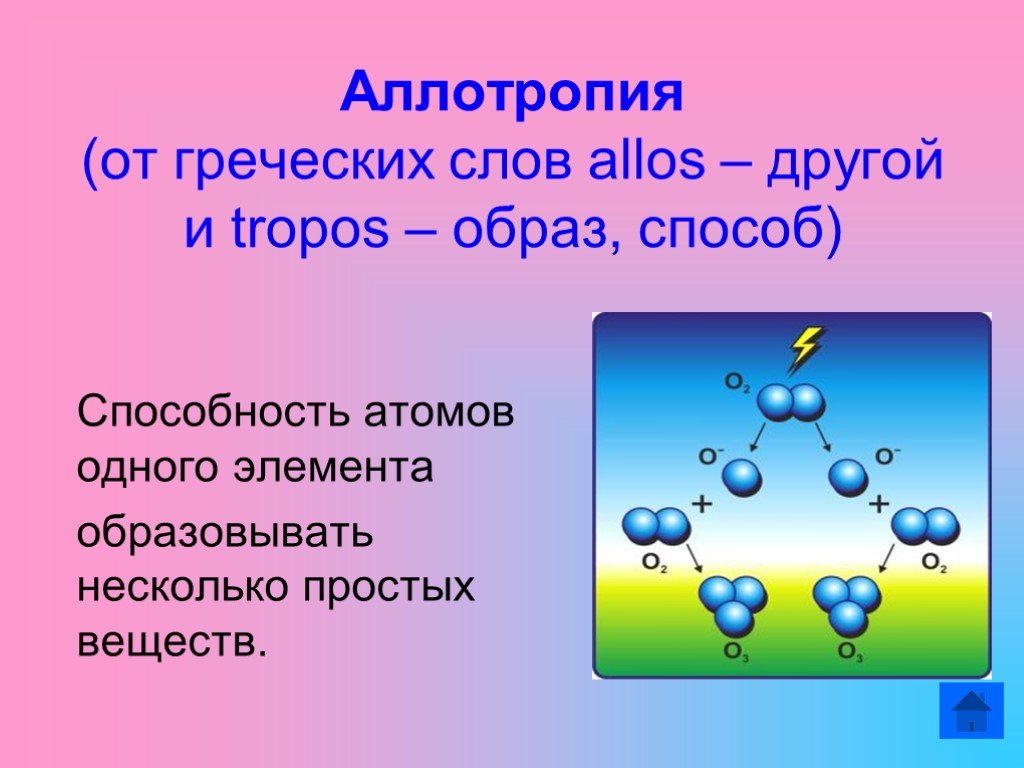
1. Элемент № 8 2. Oxygenium - Кислород 3. Джозеф Пристли 4. Карл Вильгельм Шееле 5. Антуан Лоран Лавуазье 6. Корнелиус Дреббел 7. Распространение ...Аллотропия
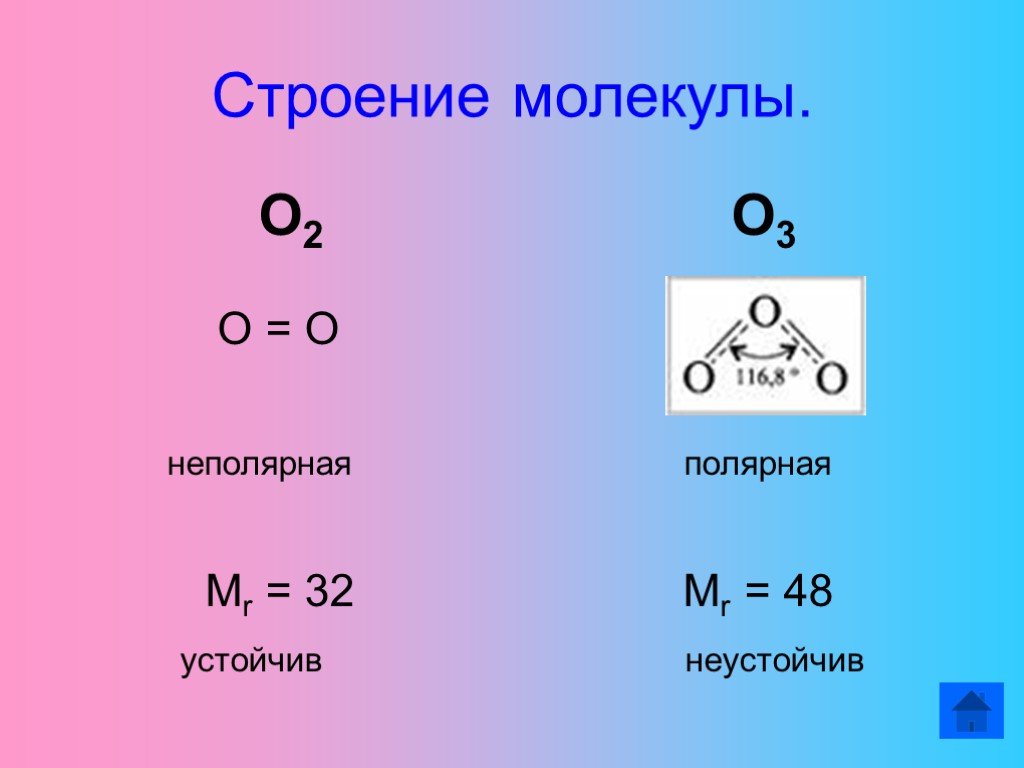
Аллотропия- это явление когда один элемент образует несколько простых веществ. 1) Аллотропия кислорода. Атомы кислорода могут образовывать кислород ...Физические свойства кислорода и его получение
Цели урока. Повторение. Новый материал. Тесты на закрепление. Рефлексия. Домашнее задание. Цели: - сформировать представление о кислороде; Задачи: ...Роль кислорода
Дыхание. Кислород необходим практически всем живым существам. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни. ...Интерактивная игра "Химия в ребусах: Химические элементы"
НИКЕЛЬ. ИОД. АЗОТ. БОР. МАГНИЙ Й. МАРГАНЕЦ. КРЕМНИЙ Л=й. МЫШЬЯК. УГЛЕРОД О. ЦИРКОНИЙ. АРГОН. МЕДЬ ДВЕ. КРИПТОН. ЗОЛОТО. СЕРА П=А. ВОДОРОД А=О Т=Д. ...Кислород химия
Общая характеристика кислорода. Химический элемент Знак элемента – О Валентность – II Относительная атомная масса - 16. Простое вещество Неметалл ...«Электролитическая диссоциация» химия
Электролитическая диссоциация. H2O. Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией. ...«Окислительно-восстановительные реакции» химия
СОДЕРЖАНИЕ:. 1. Какие реакции называются окислительно-восстановительными? 2. Что называют окислителем, восстановителем? 3. Окислительно-восстановительный ...«Нуклеиновые кислоты» химия
Цель урока: сформировать у студентов понимание взаимосвязанности и взаимозависимости веществ в клетке. Задачи урока: повторить строение и основные ...«Задачи» химия
- исследование задач по нанонауке; - ознакомление с наномиром: о достижениях нанохимии и нанотехнологии; - составление задач по нанонауке; - решение ...Конспекты
Фосфор. Аллотропия и свойства
Дата_____________ Класс_______________. Тема:. . Фосфор. Аллотропия и свойства. Цели урока:. знать строение, свойства и применение фосфора; ...Сера и ее соединения. Аллотропия серы. Сероводород. Оксиды серы
Тема: Сера и ее соединения. Аллотропия серы. Сероводород. Оксиды серы (. IV, VI. ). . Цели урока:. рассмотреть вещество «сера», аллотропию серы, ...Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы
Дата _____________ Класс ___________________. Тема: Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы. Цели урока:. ...Путешествие в страну кислорода
ПЯТИХАТСКАЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА. I. -. III. . СТУПЕНЕЙ. УРОК ХИМИИ В. 7. КЛАССЕ. «. Путешествие в страну кислорода». Подготовил ...Свойства кислорода
Свойства кислорода. Цель урока. Обучающие :. способствовать формированию знаний учащихся о кислороде, его химических свойствах;. . реакция ...Кислород, его общая характеристика. Нахождение в природе.Получение и свойства кислорода
Урок химии в 8 классе «Кислород, его общая характеристика. Нахождение в природе.Получение и свойства кислорода». Цель: . изучение и первичное осознание ...Получение и свойства кислорода
ТЕХНОЛОГИЧЕСКАЯ КАРТА МОДУЛЬНОГО УРОКА. ". Получение. и свойства. кислорода " (8 класс). Учебные. элементы. Дидактические цели. . Руководство ...Положение кислорода и серы в периодической системе химических элементов, строение их атомов. Озон – аллотропная модификация кислорода
Дата _____________ Класс ___________________. Тема: Положение кислорода и серы в периодической системе химических элементов, строение их атомов. ...Положение кислорода и серы в периодической системе химических элементов, строение их атомов. Озон-аллотропная модификация кислорода
Технологическая карта урока. . . Учитель Дьячук Е.Ю. учитель химии МБОУ СОШ №1 г.Оха Сахалинская область. Предмет. химия. . Класс. . ...Подгруппа кислорода
Урока по химии 9 класс по теме:. «Подгруппа кислорода». Составлен учителем химии. МОУ «СОШ №5 г.Кировска». Зудковой Верой Сергеевной. Цель ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:10 сентября 2018
Категория:Химия
Классы:
Содержит:18 слайд(ов)
Поделись с друзьями:
Скачать презентацию