Презентация "Основания" по химии – проект, доклад
Презентацию на тему "Основания" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 14 слайд(ов).
Слайды презентации
Список похожих презентаций
Основания, их классификация и свойства в свете теории электролитической диссоциации
Основания, их классификация и свойства в свете теории электролитической диссоциации. 1) сформировать понятие об основаниях как электролитах; 2) рассмотреть ...Основания органические и неорганические
Тема урока «Основания органические и неорганические». Цель урока:. Обобщить и систематизировать знания об основаниях. Исследовательская работа. Определите ...Основания, их классификация
NаОН, КОН, Са(ОН)2, Fе(ОН)3. :. Основания - это сложные вещества, в которых атом металла связан с одной или несколькими гидроксогруппами (ОН). Общая ...Основания и их классификация
Основания - сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (-ОН). Хорошо раст- воримые в воде основания называются ...Основания как электролиты
Сегодня на уроке вы. Повторите, что такое основания Вспомните классификацию оснований Закрепите знания о свойствах оснований Поупражняетесь в написании ...Основания
Основания – это электролиты, которые при диссоциации образуют катионы металла и гидроксид – анионы OH-. Диссоциация: NaOH = Na+ + OH- Ca(OH)2 = Ca2+ ...Основания
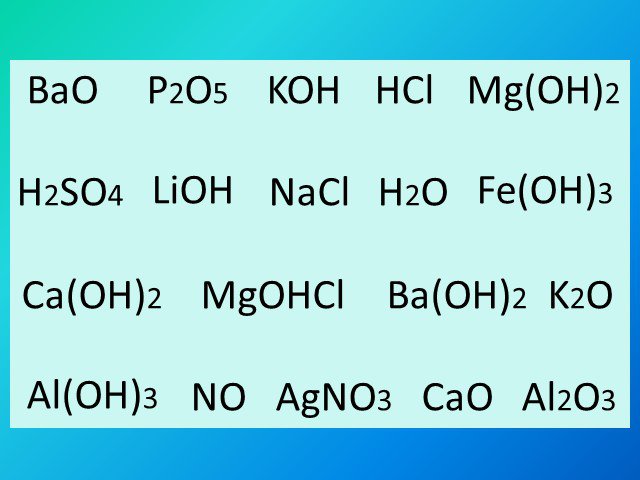
Fe(OH)3 NaOH Ca(OH)2 Al(OH)3 Cu(OH)2 Mg(OH)2. Что общего во всех этих формулах? Чем они отличаются? Основания – это сложные вещества, состоящие из ...Основания
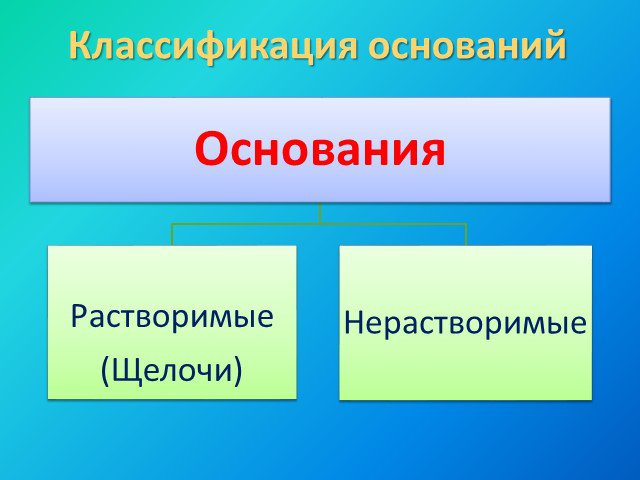
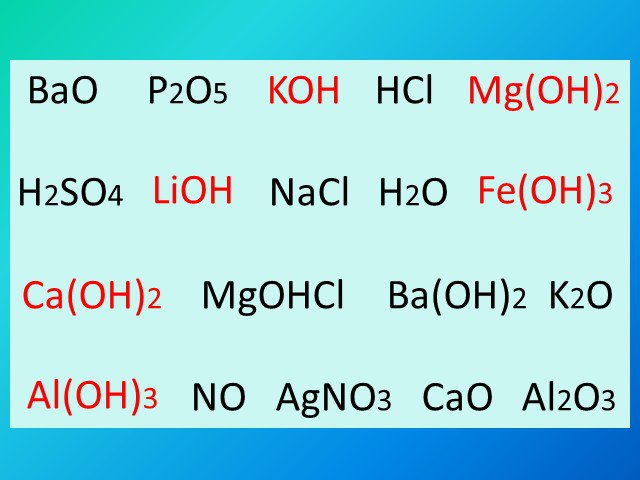
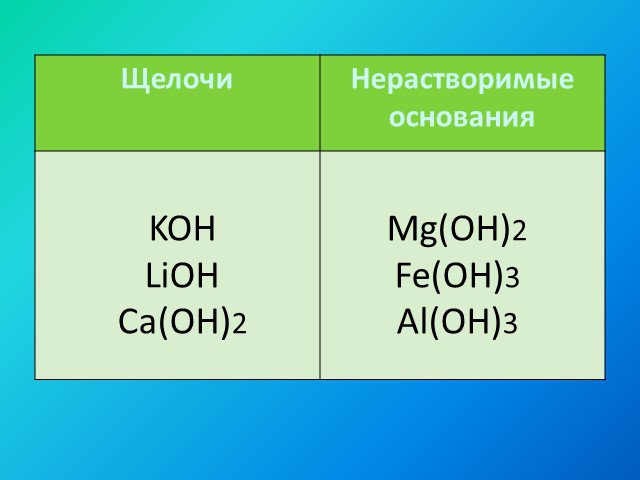
задания глоссарий содержание. физические свойства. генетическая связь. Классификация оснований. Нерастворимые. Классификация. Основания (по составу). ...Основания
Выберите из списка оксиды. Поставьте степени окисления у атомов металлов. K2O, KOH, Ca(OH)2, Fe2O3, Mn2O7, PbO2, Cl2O, Ni(OH)3, CuO, NaOH. K2O, Fe2O3, ...Основания
Основания - это…. Основания — (основные гидроксиды) — вещества, молекулы которых состоят из ионов металлов или иона аммония и одной (или нескольких) ...Основания
Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними ионов гидроксильных групп. Валентность гидроксогруппы –. Количество ...Основания
Тема урока : Основания. Основаниями называются сложные неорганические соединения состоящие из атома металла и одной или нескольких гидрооксильных ...Основания
Определение. Номенклатура. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов. M(OH)n, где M – металл, ...Основания
Основания - сложные вещества, состоящие из атомов металла, соединённых с одной или несколькими гидроксогруппами Общая формула: Me(OH)n. основания. ...Конспекты
Основания, их состав, названия. Щелочи. Индикаторы
Тема урока:. Основания, их состав, названия. Щелочи. Индикаторы. Цели урока:. -. сформировать знания о составе оснований, валентности. . гидроксильной ...Основания, их классификация и свойства
Клюкина Ольга Владимировна, учитель химии МАОУ Банниковская СОШ. . Химия 8 класс. Тема урока: «Основания, их классификация и свойства». Цели:. ...Основания, их классификация и химические свойства в свете теории электролитической диссоциации
ТЕМА УРОКА :. Основания, их классификация и химические свойства в. . свете теории электролитической диссоциации. . . II. слайд:. ЦЕЛЬ УРОКА:. ...Основания
Различные формы работы на уроке химии при изучении темы «Основания». 8 класс. Форма проведения: индивидуальная, групповая, фронтальная. Цель ...Основания, их классификация и свойства
Урок №68. Тема урока:. Основания, их классификация и свойства. Л.р.№15 «Химические свойства оснований». Цели и задачи урока:. Углубить знания ...Основания
Аннотация. Работа представляет собой демонстрационные материалы к уроку по химии для 8-го класса по теме «Основания» (Программа Гара Н.Н., 2 часа ...Основания
Конспект урока по химии 8 класс «Основания». Изварина Надежда Николаевна, учитель химии и биологии,. . МБОУ ООШ №3 г. Гуково Ростовской области. ...Основания
План-конспект урока. «Основания». Цель урока:. . . Образовательная цель: сформировать представления об новом классе неорганических соединений ...Основания
Министерство образования и науки Российской Федерации. Муниципальное бюджетное общеобразовательное учреждение. . «Средняя общеобразовательная ...Основания
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ. СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 22. Конспект урока по химии. в 8 классе. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:Алферова Мария Владимировна, учитель химии
Содержит:14 слайд(ов)
Поделись с друзьями:
Скачать презентацию