Презентация "Состав ядра атома" по физике – проект, доклад
Презентацию на тему "Состав ядра атома" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Физика. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 26 слайд(ов).
Слайды презентации
Список похожих презентаций
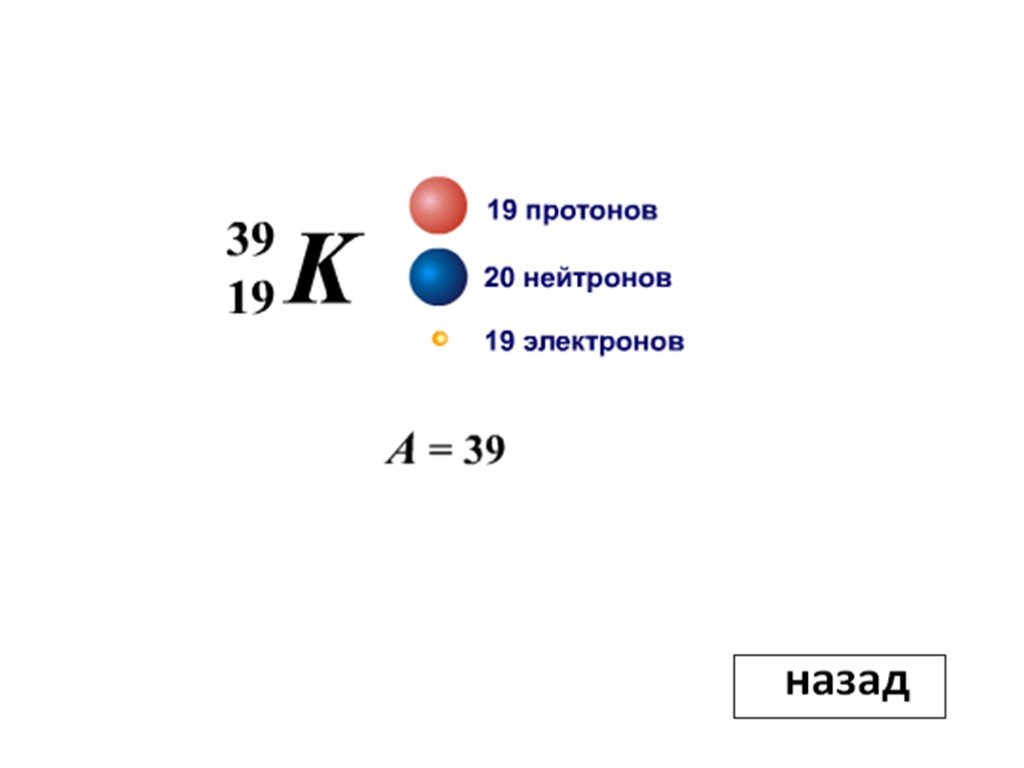
Состав атомного ядра
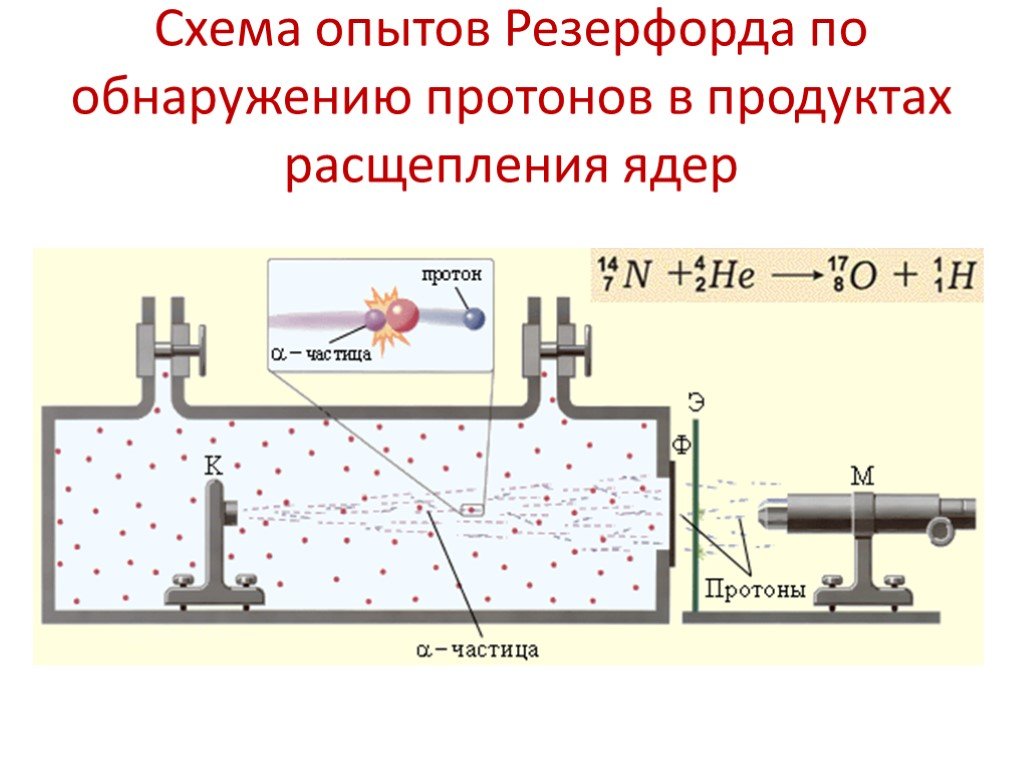
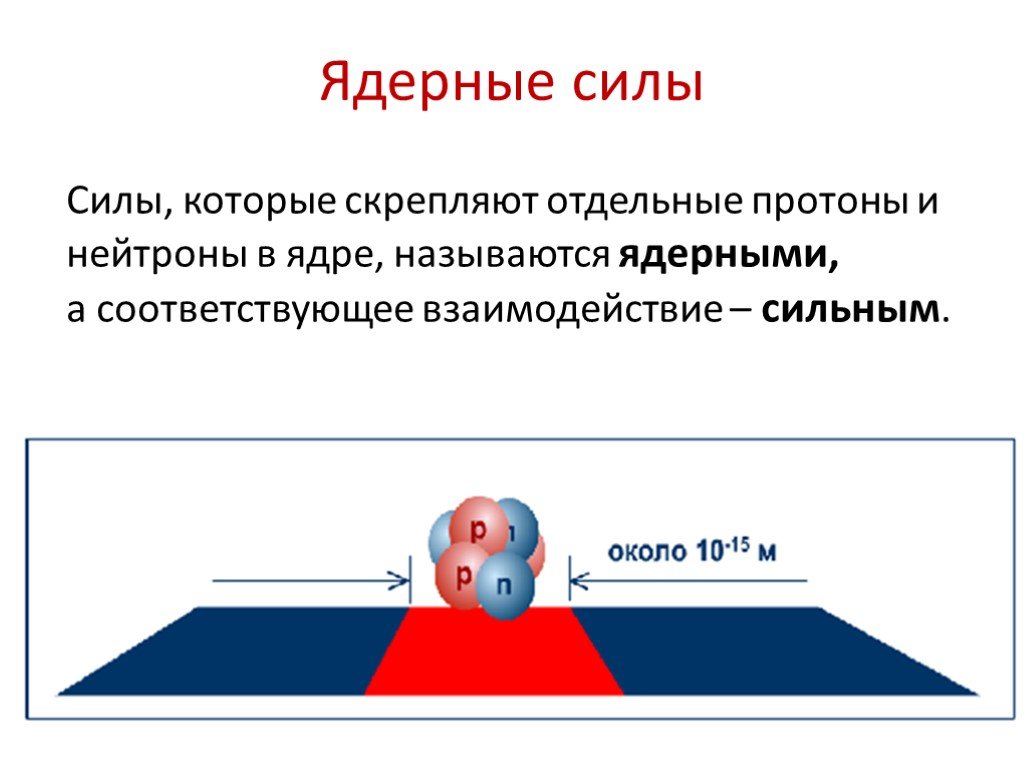
ПЛАН УРОКА. 1.Протонно-нейтронная модель строения ядер. 2.Массовое число. 3.Зарядовое число. 4.Формула обозначения ядра. 5.Примеры. 6.Ядерные силы. ...Физика атома и атомного ядра
А -18. 1.На рисунке представлен фрагмент Периодической системы элементов Д. И. Менделеева. Под названием элемента приведены массовые числа его основных ...Состав ядра. Ядерные силы
Строение атома. Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. Открыли электрон, измерили ...Теория атома Бора
Недостатки модели Резерфорда:. § 8.2. Линейчатый спектр атома водорода. ультрафиолетовая область : серия Лаймана m=1 n=2,3,4,5, видимая область спектра ...Строение атомного ядра
Атом покорен, НО цивилизация под угрозой. Прав ли был Прометей, давший людям огонь? Мир рванулся вперед, мир сорвался с пружин, Из прекрасного лебедя ...Строение атома. Квантовая теория строения атома
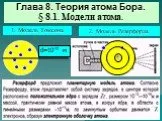
Модели атома. Модель атома Томсона Модель атома Резерфорда Модель атома Бора Модель атома Шрёдингера. Модель атома Томсона. «Пудинг с изюмом». Джозеф ...Строение атома опыт Резерфорда
Ученые древности о строении вещества. Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит из мельчайших частиц, которые ...Строение атома и опыты
Автор презентации «Строение атома» Помаскин Юрий Иванович - учитель физики МОУ СОШ№5 г. Кимовска Тульской области. Презентация сделана как учебно-наглядное ...Деление атомного ядра
. Деление ядра. . . . . ...Электронное строение атома
Порядок заполнения орбиталей электронами. VII – 7s5f6d7p 32 VI – 6s4f5d6p 32 V – 5s4d5p 18 IV – 4s3d4p 18 III – 3s3p 8 II – 2s2p 8 I – 1s 2. Е. p+ ...Открытие нейтрона. Строение атомного ядра
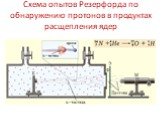
Открытие нейтрона. Ирен Жолио-Кюри (1897-1956). Фредерик Жолио-Кюри (1900-1958). При бомбардировке бериллия α-частицами обнаруживалось какое-то сильно ...Оболочечная модель ядра
При построении моделей ядра необходимо учитывать свойства сил, удерживающих протоны и нейтроны внутри ядра. Общей теории ядерных сил до сих пор не ...Модель атома Резерфорда
В 1903 году английским ученым Томсоном была предложена модель атома, которую в шутку назвали «булочкой с изюмом». По его версии атом представляет ...Модель атома
Тема 7. Модели атомов. Атом водорода по теории Бора. 7.1. Закономерности в атомных спектрах. 7.2. Ядерная модель атомов. 7.3. Элементарная теория ...Модели строения атома
Цели и задачи. Познакомить учащихся с моделями строения атома; Выяснить принципиальные отличия в строении этих моделей; Показать с помощью экспериментальных ...Модели атома
Проверка домашнего материала:. Как назвали способность атомов некоторых химических элементов к самопроизвольному излучению? Как были названы частицы, ...Физика атома
ядерная энергия - что ЭТО ? Почему мирный атом стал угрозой обществу ? Как ядерная энергия используется в медицине , технических устройствах , машинах ...Использование атома
«Атом» мирный или военный? Военный «Атом» - это в первую очередь ядерное оружие. Оно влечет за собой смерти, разрушения и не приносит благо человечеству. ...Открытия, разрушившие представление о неделимости атома
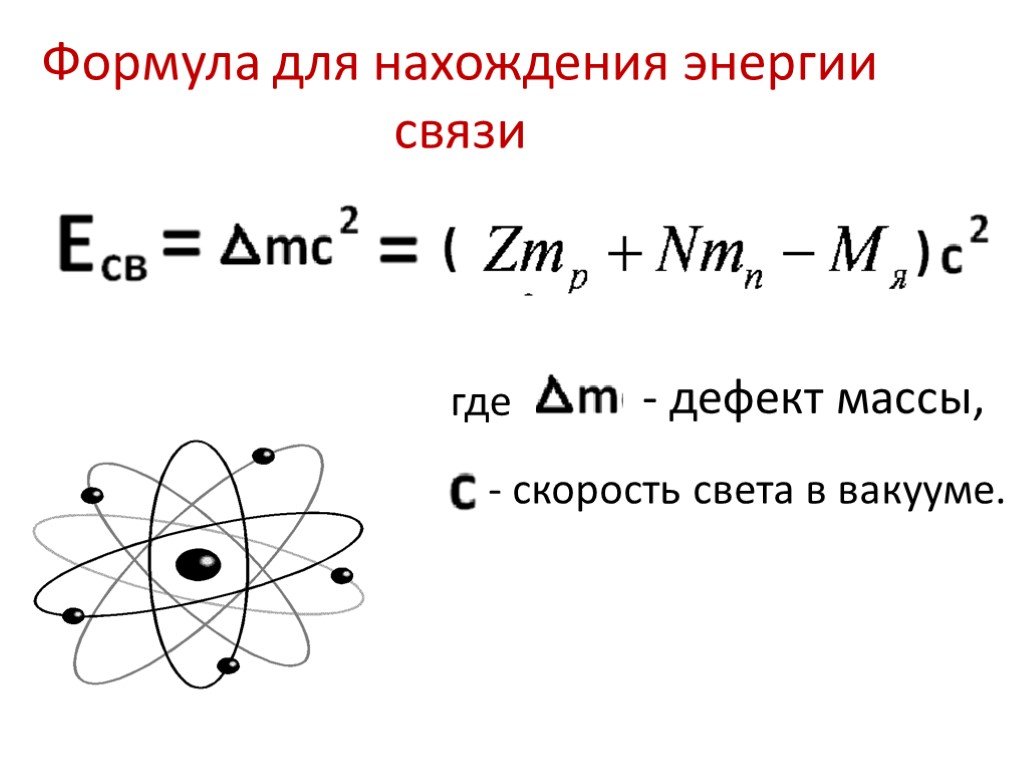
...Факты, не объяснимые существующими теориями, наиболее дороги для науки, от их разработки следует по преимуществу ожидать ее развития в ближайшем ...Энергия связи ядра и дефект масс
Дефект масс Мя126C Мя=12 а.е.м. mp=1,00759 а.е.м. mn=1,00897 а.е.м. 6·mp+6·mn=6·(1,00759 а.е.м. +1,00897 а.е.м.)=12,09936 а.е.м. 12. m=(Z·mp+(A-Z)·mn) ...Конспекты
Состав атомного ядра. Массовое число. Зарядовое число. Изотопы
Тема: Состав атомного ядра. Массовое число. Зарядовое число. Изотопы. Тип урока: Объяснение нового материала. Цели урока:. . Образовательные. ...Строение атома и атомного ядра
9 класс. . Урок № 8 в теме « Строение атома и атомного ядра». Ядерные силы, ядерные реакции. Энергия связи. Дефект масс. Цели урока : ...Открытие нейтрона. Состав атомного ядра. Массовое число. Изотопы
Нуриманов Д.Р., МКОУ СОШ №2. . Проект открытого урока. . «Открытие нейтрона. Состав атомного ядра. Массовое число. Изотопы». Цель:. Формирование ...Ядерные реакции. Деление ядра урана. Цепная ядерная реакция
Урок № 62-169 Ядерные реакции. Деление ядра урана. Цепная ядерная реакция. . Д/з: 22.16-22.18[1] Подготовка докладов консультантами. Ядерные реакции. ...Строение атомного ядра
Урок физики в 9 классе. Тема: Строение атомного ядра. Цель урока:. познакомить учащихся с протонно-нейтронной моделью ядра, научить обобщать и ...Строение атома
Тема. «Строение атома». . 8 класс. Цели для ученика:. Общая цель. :. совершенствовать. знания об электрических явлениях. Образовательные задачи. ...Строение атома
Муниципальное бюджетное общеобразовательное учреждение. «Авнюгская средняя общеобразовательная школа». Верхнетоемского района Архангельской области. ...Ренессанс «мирного атома
Повторительно - обощающий урок по теме:. «Ренессанс «мирного атома» или его закат?». (11 класс). “Знание становится живым, если оно применяетсядля ...Путешествие в страну атомного ядра
. Разработка открытого урока по физике в 11А профильном физико – математическом классе. «Путешествие в страну атомного ядра». Урок подготовила. ...Путешествие в мир атома
Клюшина Ж.В.,. . учитель физики МБОУ СОШ №37. . г. Шахты Ростовской области. Тема урока: «Путешествие в мир атома». Цели урока:. Образовательные:. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:24 сентября 2018
Категория:Физика
Содержит:26 слайд(ов)
Поделись с друзьями:
Скачать презентацию