Слайд 2Обобщение и систематизация знаний по теме " Подгруппа углерода"
Решение задач и упражнений по теме "Подгруппы углерода"
Слайд 3На этом занятии мы закрепим и обобщим знания об элементах – углероде и кремнии. Выполняя предложенные задания, вы повторите свойства простых веществ, состоящих из атомов этих элементов, химические свойства изученных соединений углерода и кремния, уравнения соответствующих реакций. Дадите характеристику элементам подгруппы углерода, вспомните, как определять карбонат- силикат- ионы и углекислый газ; решать комбинированные задачи.
Слайд 4Часть 1. Общая характеристика главной подгруппы четвертой группы.
Главную подгруппу IV группы периодической системы Д. И. Менделеева образуют пять элементов - углерод, кремний, германий, олово и свинец. элемент С Si Ge Sn Pb Радиус атома 2,50 1,74 2,02 1,72 1,55
В подгруппе с ростом порядкового номера элемента увеличивается атомный радиус, неметаллические свойства ослабевают, а металлические усиливаются
Слайд 5Среди элементов IV группы наибольшее значение имеют углерод, входящий в состав всех живых организмов, и кремний - важнейший элемент земной коры.
Алмаз и графит кремний (модификации углерода) – неметаллы
Слайд 6Уже у германия проявляются металлические свойства. Германий по внешнему виду похож на металлы, но хрупок. Как и кремний, германий принадлежит к полупроводникам, т. е. к веществам, занимающим промежуточное положение между изоляторами, к которым относятся многие неметаллы), и проводниками -металлами.
Слайд 7олово и свинец - металлы.
Слайд 8Задание 1.
Зарисуйте схемы электронного строения атомов углерода и кремния . Объясните, почему элементы подгруппы углерода образуют оксиды общей формулы RO2 и RO, а водородные соединения углерода и кремния имеют формулу RН4. Каков характер этих соединений?
Слайд 9Решение: Подсказка 1
Элементы главной подгруппы четвертой группы : р-элементы IV группы периодической системы Д.И. Менделеева.
На внешнем электронном слое атомы этих элементов имеют 4 электрона: 2s- и 2 р- электрона. Такая электронная структура записыватся. как ns2np2.
Теперь вспомните , как зарисовать схемы электронного строения атомов углерода и кремния .
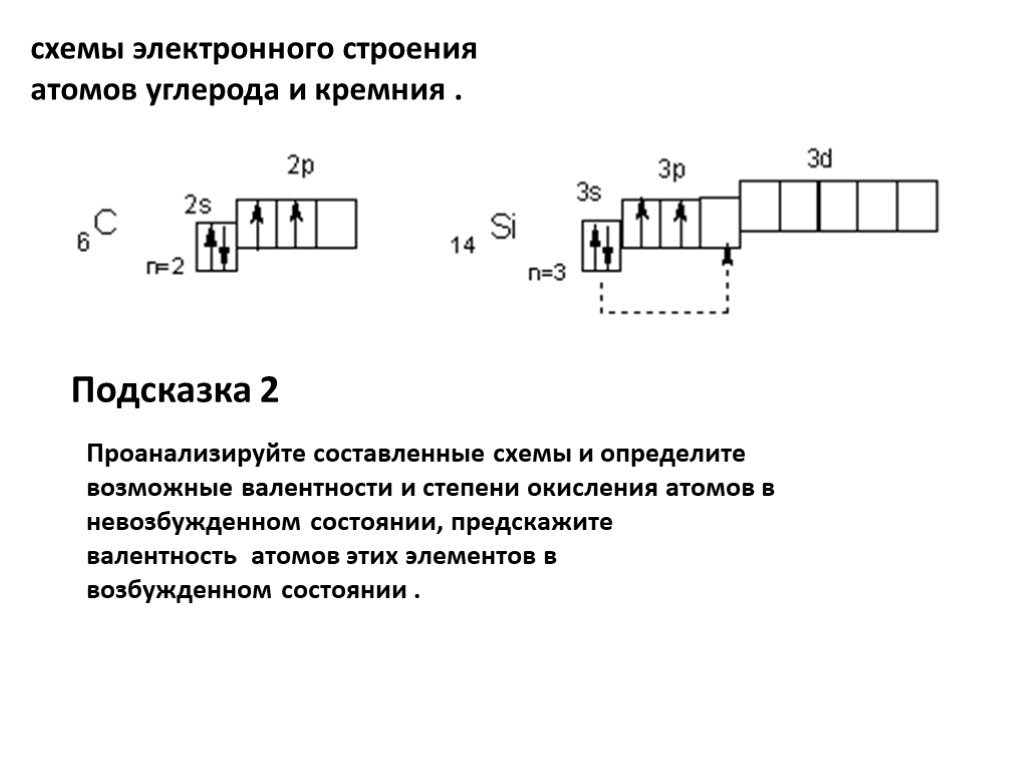
Слайд 10схемы электронного строения атомов углерода и кремния .
Подсказка 2
Проанализируйте составленные схемы и определите возможные валентности и степени окисления атомов в невозбужденном состоянии, предскажите валентность атомов этих элементов в возбужденном состоянии .

Слайд 11В невозбужденном состоянии их атомы имеют по 2 неспаренных электрона. Следовательно, в нормальном состоянии элементы этой подгруппы отдают 2 электрона и проявляют степень окисления +2 С° - 2ē → С+2 степень окисления в СО
При переходе в возбуждённое состояние, сопровождающееся переходом одного из s – электронов внешнего слоя в свободную ячейку p – подуровня того же уровня.(показано пунктирными стрелками), все электроны наружного слоя становятся не спаренными и валентность при этом возрастает до 4. Эти неспаренные 4 электрона могут участвовать в образовании 4 связей.
В таких соединениях элементы могут проявлять степени окисления как +4 (с атомами более электроотрицательных элементов), так и -4 (с атомами менее электроотрицательных элементов),. С° + 4ē → С-4 низшая степень окисления (СН4). С° - 4ē → С+4 высшая степень окисления (СО2).
Поэтому элементы подгруппы углерода образуют оксиды общей формулы RO2 и RO, а водородные соединения углерода и кремния имеют формулу RН4.

Слайд 12Подсказка 3
Для того , чтобы дать полный ответ , вспомните , что в подгруппе с ростом порядкового номера элемента увеличивается атомный радиус, неметаллические свойства ослабевают, а металлические усиливаются. Вспомните, каков характер высших оксидов металлов и неметаллов? Характерны ли для металлов отрицательные степени окисления?
Оформите свое решение в виде таблицы.
Слайд 13В соединениях элементы подгруппы углерода проявляют степень окисления +4 и -4, а также +2, причем последняя с увеличением заряда ядра становится более характерной. Для углерода, кремния и германия наиболее типична степень окисления +4, для свинца +2. Высшим оксидам соответствует степень окисления +4 . Высшие оксиды углерода и кремния обладают кислотными свойствами, оксиды остальных элементов подгруппы - амфотерны .
Слайд 14Задание 2
Среди карбидов и силицидов особое место занимает карборунд SiC, который можно назвать как карбидом кремния, так и силицидом углерода. Карборунд имеет высокую температуру плавления, благодаря алмазоподобной структуре; его твердость близка к твердости алмаза. Химически SiC очень стоек. Определите степень окисления каждого из элементов в этом веществе.
Слайд 15Решение: Подсказка
Вспомните , как меняется электроотрицательность элементов по подгруппе с возрастанием порядкого номера. Определите , какой из элементов будет проявлять отрицательную, а какой положительную степень окисления.
Слайд 16Углерод и кремний - это неметаллы, так как на внешнем электронном слое 4 электрона. Но так как кремний имеет больший радиус атома, то для него более характерна способность отдавать электроны, чем для углерода. Поэтому в этом соединении углерод имеет отрицательную степень окисления -4, а кремний положительную +4.
Слайд 17Тесты
ТЕСТ 2. На внешнем электронном уровне атома углерода находится 6 электронов. 1.Да 2.Нет ТЕСТ 3. Кремний – второй по распространенности элемент на Земле после кислорода. 1. Да 2. Нет
ТЕСТ 4. Кремний относится к металлам.. 1.Да 2.Нет
ТЕСТ 1 . В подгруппе с ростом порядкового номера элемента неметаллические свойства усиливаются 1. Да 2. Нет
ТЕСТ 5 . Валентность углерода в высшем оксиде и летучем водородном соединении совпадает. 1. Да 2. Нет
Слайд 18Ответы Да Нет Да Нет Да
Слайд 19Часть 2.
Простые вещества, образованные атомами углерода и кремния. Их химические свойства .
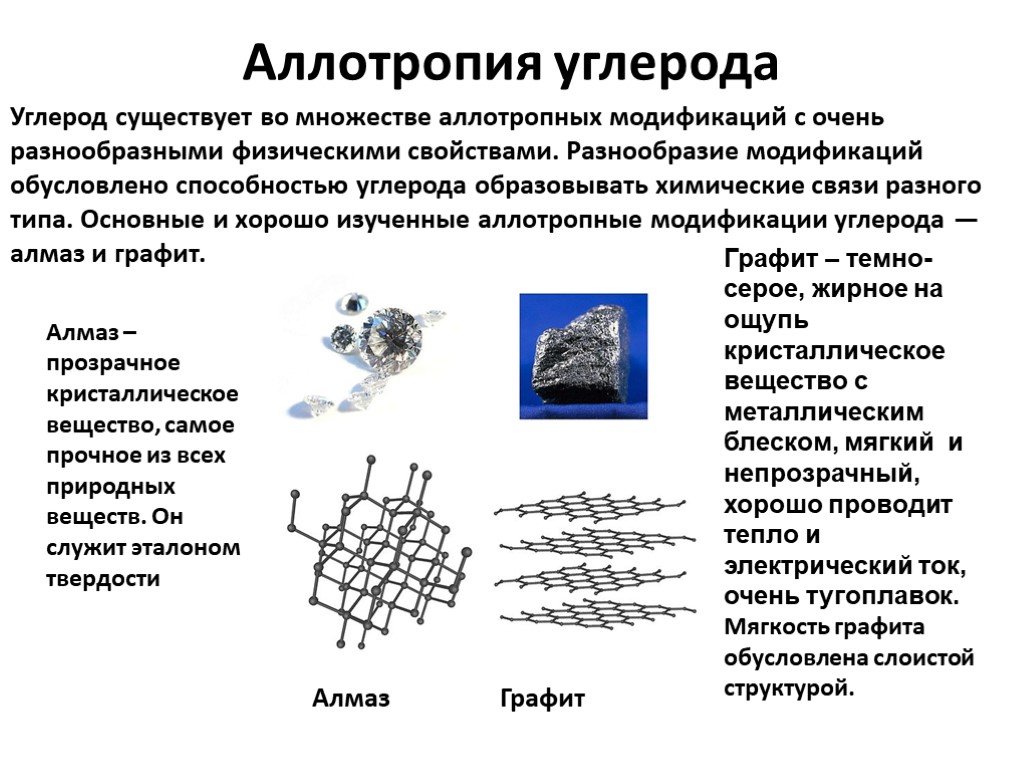
Слайд 20Аллотропия углерода
Алмаз Графит
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа. Основные и хорошо изученные аллотропные модификации углерода — алмаз и графит.
Алмаз – прозрачное кристаллическое вещество, самое прочное из всех природных веществ. Он служит эталоном твердости
Графит – темно-серое, жирное на ощупь кристаллическое вещество с металлическим блеском, мягкий и непрозрачный, хорошо проводит тепло и электрический ток, очень тугоплавок. Мягкость графита обусловлена слоистой структурой.

Слайд 21У графита атомы углерода расположены параллельными слоями. Расстояние между соседними слоями гораздо больше, чем между соседними атомами в слое. Это обусловливает малую прочность связи между слоями, и поэтому графит легко расщепляется на тонкие чешуйки, которые сами по себе очень прочные.
В кристаллической решетке алмаза каждый атом углерода окружен четырьмя другими. Атомы расположены на одинаковых расстояниях друг от друга и очень прочно связаны между собой ковалентны-ми связями. Этим объясняется большая твердость алмаза.

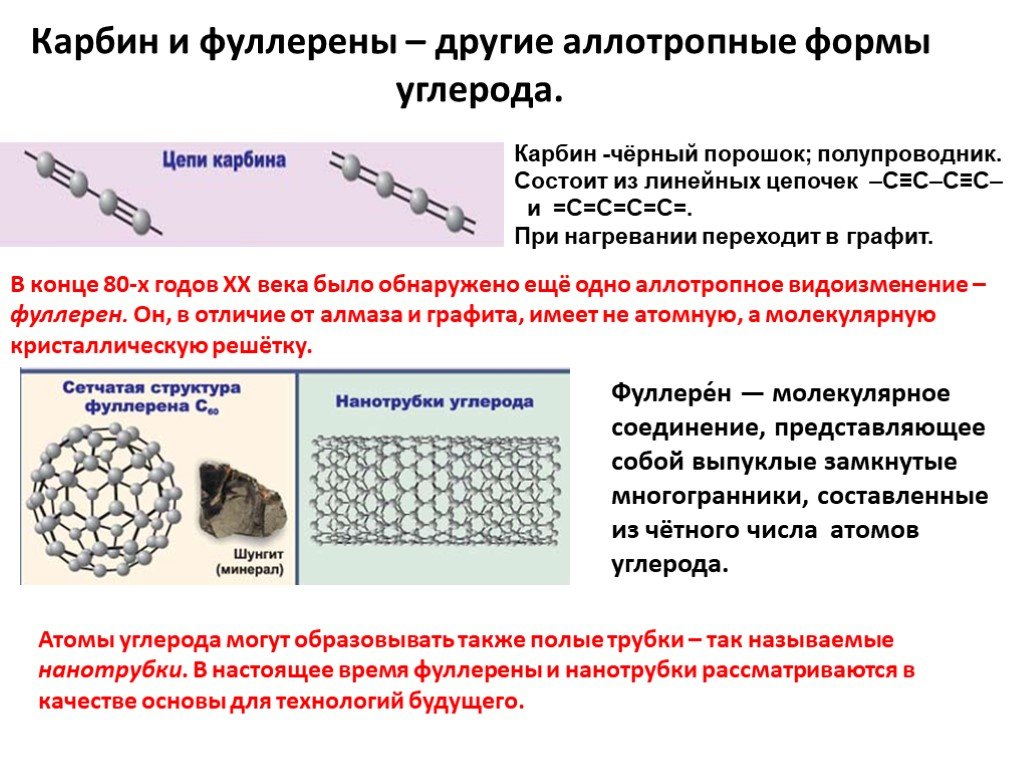
Слайд 22Карбин и фуллерены – другие аллотропные формы углерода.
Карбин -чёрный порошок; полупроводник. Состоит из линейных цепочек –C≡C–C≡C– и =С=С=С=С=. При нагревании переходит в графит.
Фуллере́н — молекулярное соединение, представляющее собой выпуклые замкнутые многогранники, составленные из чётного числа атомов углерода.
В конце 80-х годов XX века было обнаружено ещё одно аллотропное видоизменение – фуллерен. Он, в отличие от алмаза и графита, имеет не атомную, а молекулярную кристаллическую решётку.
Атомы углерода могут образовывать также полые трубки – так называемые нанотрубки. В настоящее время фуллерены и нанотрубки рассматриваются в качестве основы для технологий будущего.

Слайд 23Аморфный углерод и его сорта.
Графит, алмаз известны с древности Однако определенно утверждать можно лишь одно: до алмаза и до графита было открыто вещество, которое еще несколько десятилетий назад считали аморфной формой элементарного углерода - уголь.
Бурые угли – твердые горючие ископаемые, образовавшиеся из торфа. Содержат 65-70% углерода, имеют бурый цвет.
Каменный уголь – вид ископаемого топлива, образовавшийся под землёй при глубоком разложении растительных остатков без доступа кислорода.Содержание углерода в каменном угле в зависимости от месторождения составляет от 75% до 95%.
Древе́сный у́голь — микропористый высокоуглеродистый продукт, образующийся при разложении древесины без доступа воздуха.
Слайд 24Аморфный углерод – не является еще одним аллотропным видоизменением углерода, а представляет собой мелкокристаллический графит.
Слайд 25Аллотропия кремния
Различают две основные аллотропные модификации кремния - аморфную и кристаллическую. Решётка кристаллической модификации кремния - атомная, алмазоподобная. , но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твёрдость кремния значительно меньше, чем алмаза.
Кристаллическая структура кремния.
Также выделяют поликристаллический и монокристаллический кремний. Аморфный кремний – порошок бурого цвета на основе сильно разупорядоченной алмазоподобной структуры.
Поликристаллический кремний
Слайд 26Задание 3.
Как доказать, что графит и алмаз являются аллотропными видоизменениями одного и того же химического элемента? Чем объяснить различия их свойств?
Слайд 27Вспомните, как отличаются химические свойства веществ, являющихся аллотропными модификациями одного и того же элемента.
Слайд 28Запишите уравнение реакции горения алмаза и углерода. Как доказать, что в обоих случаях получается один и тот же продукт реакции?
Слайд 29И алмаз, и графит при сгорании в кислороде образуют оксид углерода (IV) СО2, при пропускании которого через известковую воду выпадает белый осадок карбонат кальция СаСО3. С + О2 = СО2; СО2 + Са(ОН)2 = CaCO3 + Н2О. Кроме того, из графита можно получить алмаз при нагревании под высоким давлением. Следовательно, в состав и графита, и алмаза входит только углерод. Различие в свойствах графита и алмаза объясняется различием в строении кристаллической решетки.
Слайд 30Химические свойства простых веществ, образованных атомами углерода и кремния .
При обычных условиях углерод и кремний очень инертны и практически не взаимодействуют ни с какими простыми и сложными веществами. Графит и кремний — типичные восстановители При нагревании с избытком воздуха графит и кремний образуют диоксиды: С + О2 = СО2, Si + О2 = SiO2,
Слайд 31Графит и кремний — типичные восстановители . Уже при обычной температуре углерод и кремний реагируют со фтором, образуя тетрафториды СF4 и SiF4, при нагревании — с хлором, давая СCl4 и SiCl4. При более сильном нагревании углерод и кремний реагируют с серой и азотом: 4С + S8 = 4СS2, 2С + N2 = С2N2, 4Si + S8 = 4SiS2 и даже между собой, образуя карборунд — вещество, по твердости близкое к алмазу: Si + С = SiC.
Слайд 32Восстановительные свойства графита и кремния в реакциях со сложными веществами.
С водой углерод и кремний реагируют лишь при высоких температурах: С + Н2О = СО + Н2 Si + ЗН2О = Н2SiO3 + 2Н2 Первая из этих реакций имеет большое практическое значение. Она лежит в основе процесса газификации твердого топлива.
Слайд 33Графит часто используют для восстановления малоактивных металлов из их оксидов: СuО + С = Сu + СО↑. При нагревании же с оксидами активных металлов углерод и кремний диспропорционируют, образуя карбиды СаО + 3С = СаС2 + СО↑, 2Аl2О3 + 9С = Аl4С3 + 6СО↑ или силициды 2МgО + 3Si = Мg2Si + 2SiO2.
Слайд 34Обычные кислоты на углерод и кремний не действуют, тогда как концентрированные Н2SО4 и НNО3 окисляют углерод: С + 2Н2SО4 = СО2↑+ 2SО2↑ + 2Н2О, 3С + 4НNO3 = 3СО2↑ + 4NO↑ +2Н2О. Кроме того, кремний растворяется в водных растворах щелочей: Si + 2NaОН + Н2О = Na2SiO3 + Н2↑.
Слайд 35Задача 4.
Смесь кремния и угля, массой 5,0 г, обработали избытком концентрированного раствора щелочи при нагревании. В результате реакции выделилось 2,8 литров водорода (н.у.). Вычислите массовую долю углерода в этой смеси.
Слайд 36Подсказка 1.
Если по условию задачи известны массы или объемы веществ необходимо рассчитать количества этих веществ (моль). Далее необходимо записать уравнения протекающих реакций и провести расчет количеств веществ, участвующих в реакции.
Слайд 37v(Н2) = 2,8/22,4 = 0,125 моль.
рассчитаем количество вещества водорода (моль).
С раствором щелочи реагирует только кремний: Si + 2NаОН + Н2О = Na2SiO3 + 2Н2↑. Рассчитаем количество кремния по данному уравнению реакции. Очевидно, что оно в 2 раза меньше, чем количество вещества водорода : v(Si) = 0,125/2 = 0,0625 моль. Найдем массу прореагировавшего кремния: М(Si) =28 г/моль ( молярная масса кремния) m(Si) = 0,025.28 = 1,75 г. m(С) = 5,0-1,75 = 3,25 г. Массовая доля углерода равна: ω(С) = 3,25/5,0 = 0,65, или 65%. Ответ. 65% С.
Слайд 38Задание 5.
Объясните окислительно-восстановительные процессы с участием кремния, показав переходы электронов методом электронного баланса. Si + НNО3 + НF = SiF4↑ + NO↑ +Н2О. Si + NaОН + Н2О = Na2SiO3 + Н2↑. Расставьте коэффициенты .
Слайд 39Расставим степени окисления и определим атомы элементов, участвующие в процессе окисления-восстановления.
Слайд 40Кремний растворяется в смеси концентрированных азотной и плавиковой кислот: Si 0+ НN+5О3 + НF = Si+4F4↑ + N+2O↑ +Н2О. Применим метод электронного баланса:
Расставим полученные коэффициенты: 3Si + 4НNО3 + 12НF = 3SiF4↑ + 4NO↑ +8Н2О.
Слайд 41Кремний растворяется в водных растворах щелочей Расставим степени окисления и опредилим атомы элементов, участвующие в процессе окисления-восстановления: Si 0+ 2NaОН + Н+2О = Na2Si+4O3 + Н02↑. Применим метод электронного баланса:
Расставим полученные коэффициенты: Si + 2NaОН + Н2О = Na2SiO3 + 2Н2↑.
Слайд 42Кремний растворяется в смеси концентрированных азотной и плавиковой кислот и в водных растворах щелочей, поскольку относится к типичным восстановителям . В обеих реакциях атом кремния отдает 4 электрона, образуя устойчивые соединения со степенью окисления +4 - Si+4F4↑ и Na2Si+4O3.
Слайд 43Окислительные свойства углерода и кремния.
Активные металлы — более сильные восстановители, чем углерод или кремний, поэтому последние при непосредственном взаимодействии с ними выступают в качестве окислителей. Получение: Са + 2С = СаС2, 2Mg + Si = Мg2Si. Соединения углерода и кремния с металлами — карбиды и силициды, помимо рассмотренных реакций получают также взаимодействием кремния с гидридами металлов, например: 2СаН2 + Si = Са2Si + 2Н2↑. Все эти реакции протекают при высоких температурах.
Слайд 44Свойства карбидов и силицидов.
Большинство карбидов активно реагируют с водой (тем более с кислотами), выделяя соответствующие углеводороды: СаС2 + 2Н2О = Са(ОН)2 + С2Н2↑, Al4C3 + 12H2O = 4Al(OH)3↓ + 3CH4↑, В отличие от карбидов, с водой и кислотами взаимодействуют лишь силициды щелочных или щелочноземельных металлов, выделяя простейшее водородное соединение кремния моносилан, которое чаще всего называют просто силан SiН4: Са2Si + 4НСl = 2СаСl2 + SiН4↑.
Слайд 45Свойства силана.
Силан — бесцветный газ, имеющий запах плесени, самопроизвольно воспламеняющийся на воздухе, сгорая до SiO2 и воды: SiН4 + 2О2 = SiO2 + 2Н2О. При нагревании выше 400 °С без доступа воздуха силан распадается на кремний и водород (один из способов получения кремния): SiН4 = Si + 2Н2↑. Щелочи очень легко разлагают силан по уравнению: SiН4 + 2КОН + Н2О = К2SiO3 + 4Н2↑,
Слайд 46Получение метана.
Углерод в отличие от кремния непосредственно взаимодействует с водородом: С + 2Н2 = СН4 — метан Реакция осуществляется при нагревании в присутствии катализатора (мелкий раздробленный никель).
Слайд 47Задание 6.
«Встретились два богатыря, равные по силе, одинаковые по массе, чуть тяжелее воздуха. Начали они бороться, и осталось от них мокрое место на песке...». О каких химических «богатырях» идёт речь?
Слайд 48Подсказка .
Мокрое место на песке...-предположим, что имеется в виду смесь песка и воды , т.е. продукты химической реакции SiO2 + Н2О. Попробуйте предположить каковы исходные вещества этой реакции.
Слайд 49Уравнение химической реакции можно представить, как Х + Y = SiO2 + Н2О. Найдем Х и Y , очевидно, что эти вещества содержат атомы Si ,Н и О . Предположим, что Y это O2, М (O2) = 32 г/моль, т.е. М(Х) = 32 г/моль Х это силан SiН4 Запишем уравнение химической реакции : SiН4 + 2О2 = SiO2 + 2Н2О.
Ответ: В условии задачи описана реакция горения силана в кислороде. Два богатыря это SiН4 и O2.
Слайд 50ТЕСТ 1. Алмаз отличается высокой твердостью; он самый твердый из известных веществ. 1.Да. 2.Нет. ТЕСТ 2. Алмаз отличается от графита физическими свойствами. 1.Да. 2.Нет. ТЕСТ 3. Углерод в окислительно -восстановительной реакции может только окисляться 1.Да 2.Нет ТЕСТ 4. Углерод и кремний восстановливают металлы из их оксидов. 1.Да 2.Нет ТЕСТ 5. Каменный уголь состоит только из атомов углерода . 1. Да 2. Нет ТЕСТ 6 . При нагревании угля с оксидом железа (III) образуется железо. 1. Да 2. Нет
Слайд 51Да Да Нет Да Нет Да
Слайд 52Часть 3.
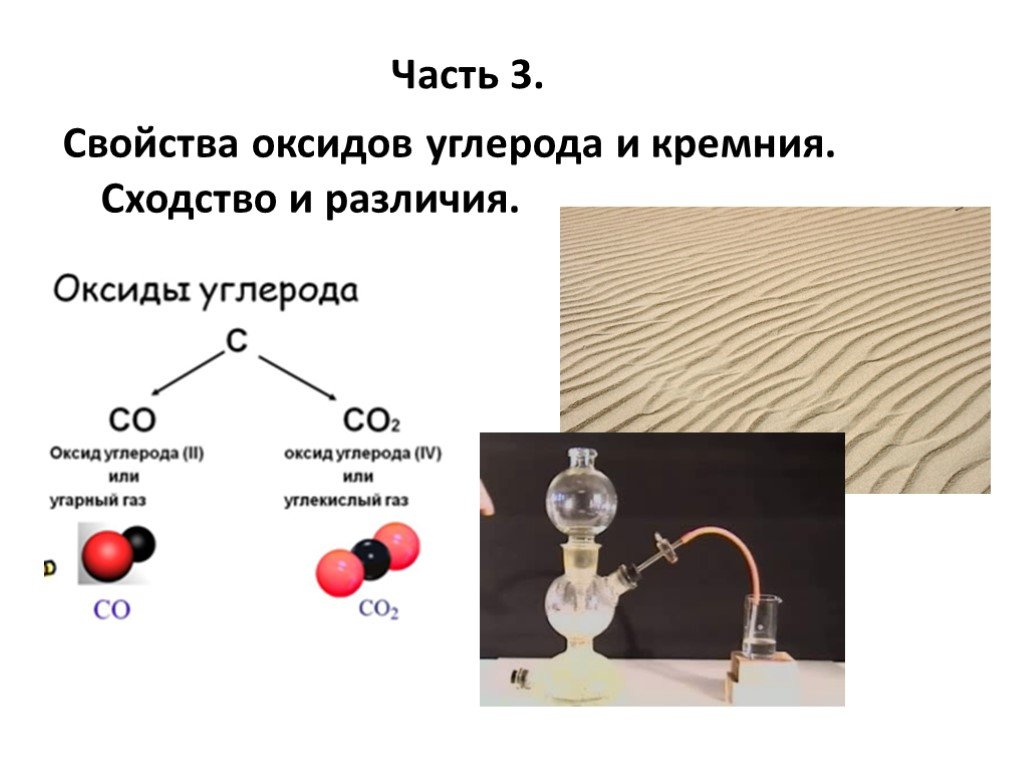
Свойства оксидов углерода и кремния. Сходство и различия.
Слайд 53Оксид углерода (II) и оксид кремния (II).
При нагревании на воздухе углерод и кремний сгорают с образованием оксидов. Однако процессы окисления идут по-разному.
Кремний с кислородом во всех случаях образует оксид кремния (IV). Оксид кремния (II) может быть получен лишь косвенным путем: Si + SiO2 = 2SiO. Они оба не реагируют при обычных условиях ни с кислотами, ни со щелочами. В отличие от угарного газа СО, оксид кремния (II) мало доступен и очень редко используется,
2С + О2 = 2СО который образуется также при нагревании простых веществ с их диоксидами: С + СО2 = 2СО
При недостатке кислорода углерод образует оксид углерода (II), а при избытке — оксид углерода (IV).

Слайд 54Оксид кремния (IV) и оксид углерода (IV)
Кристалл кварца и его атомная кристаллическая решетка.
В природе кремнезем(SiO2) встречается в виде включений в граниты и другие породы. Такие включения заметны на осколках породы, они напоминают кусочки оплавленного стекла. Освобождаясь при выветривании породы, они скапливаются в руслах рек в виде белого песка. Иногда и в виде прекрасных кристаллов размером, иногда превышающим человеческий рост.
Оксид кремния SiO2 - твердое, очень тугоплавкое вещество (температура плавления более 1700 °С), широко распространенное в природе.

Слайд 55Оксид углерода (IV) (диоксид углерода, углекислый газ) - газ без цвета и запаха, не поддерживающий дыхания и горения, тяжелее воздуха.
Высшие солеобразующие оксиды углерода и кремния довольно сильно отличаются по свойствам. Оксид углерода (IV) - газ, который конденсируется лишь при сильном охлаждении, образуя кристаллическую массу.
Оксид кремния (IV) практически нерастворим в воде.
Оксид углерода (IV) растворяется в воде (1:1 по объему), причем он частично взаимодействует с ней, образуя угольную кислоту: СO2 + Н2О = H 2СO3
«Сухой лёд» — твёрдый CO2, при обычных условиях (атмосферном давлении и комнатной температуре) переходящий в парообразное состояние, минуя жидкую фазу.
твердый углекислый газ имеет молекулярную решетку: t°пл.= -78,5°
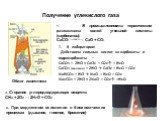
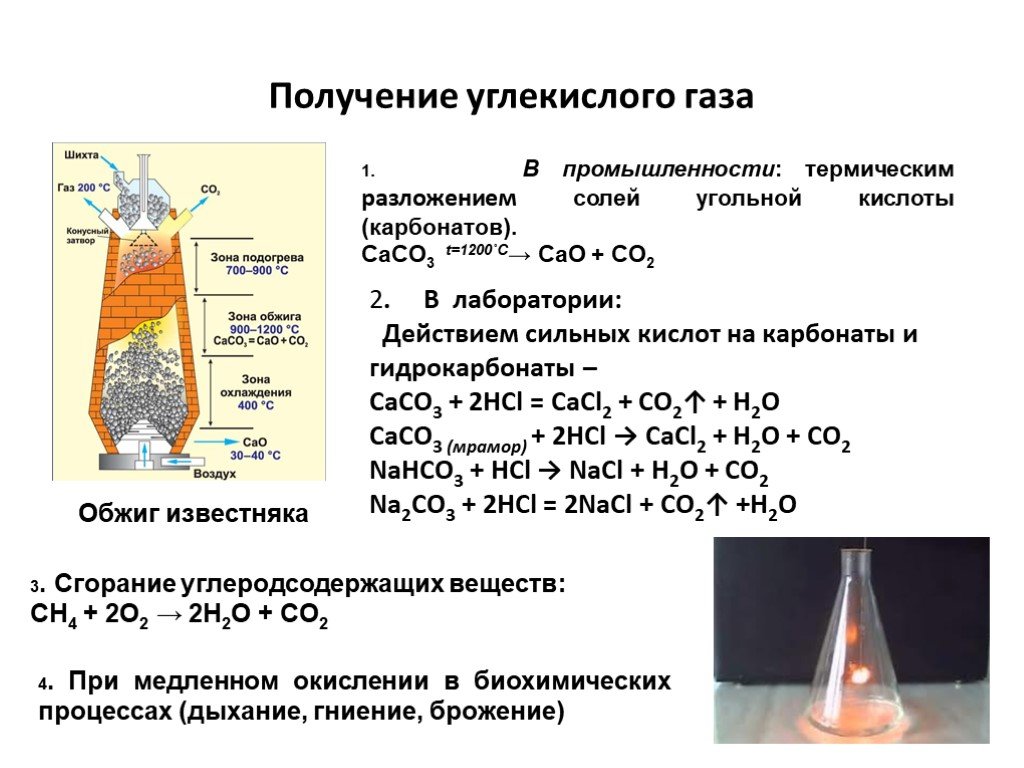
Слайд 56Получение углекислого газа
1. В промышленности: термическим разложением солей угольной кислоты (карбонатов). CaCO3 t=1200˚C→ CaO + CO2
Обжиг известняка
2. В лаборатории: Действием сильных кислот на карбонаты и гидрокарбонаты – CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O CaCO3 (мрамор) + 2HCl → CaCl2 + H2O + CO2 NaHCO3 + HCl → NaCl + H2O + CO2 Na2CO3 + 2HCl = 2NaCl + CO2↑ +H2O
3. Сгорание углеродсодержащих веществ: СН4 + 2О2 → 2H2O + CO2
4. При медленном окислении в биохимических процессах (дыхание, гниение, брожение)
Слайд 57Качественная реакция на углекислый газ:
Углекислый газ можно обнаружить при помощи известковой воды. При его пропускании, например так, как показано на рисунке, происходит помутнение известковой воды Ca(OH)2 за счёт образования белого осадка – нерастворимой соли CaCO3:
Ca(OH)2 + CO2 → CaCO3 ↓+ H2O
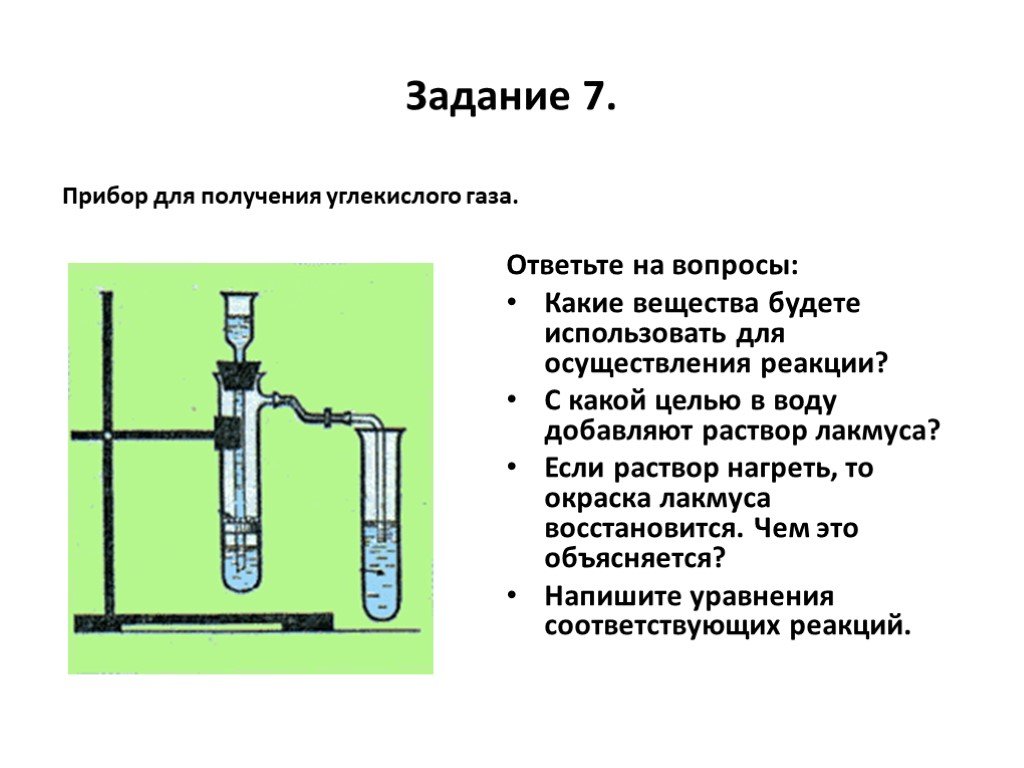
Слайд 58Задание 7.
Ответьте на вопросы: Какие вещества будете использовать для осуществления реакции? С какой целью в воду добавляют раствор лакмуса? Если раствор нагреть, то окраска лакмуса восстановится. Чем это объясняется? Напишите уравнения соответствующих реакций.
Прибор для получения углекислого газа.
Слайд 59Вспомните , как с помощью кислоты можно доказать , что минерал имеет карбонатную (известковую ) природу. Запишите уравнение реакции.
Слайд 60Решение
Для получения углекислого газа в лаборатории используют нерастворимые карбонаты ( например, карбонат кальция) и соляную кислоту . СаСO3 + 2 HCl = СO2 + Н2О + СаCl2 Пробирка для реакции заполняется кусочками мрамора, а через воронку сверху приливается разбавленная соляная кислота
Слайд 61Вспомните каков характер гидроксида, образующегося при взаимодействии кислотного оксида с водой. Какие индикаторы могут подтвердить этот характер. Является ли полученный гидроксид устойчивым? Запишите уравнение обратимой реакции.
Слайд 62Оксид углерода (IV) растворяется в воде с образованием очень слабой- угольной кислоты, что и обнаруживается с помощью индикаторов-лакмуса или метилоранжа, меняющих окраску на красную в присутствии кислоты. СO2 + Н2О = H2СO3 – красная окраска лакмуса.
Угольная кислота очень неустойчива и при нагревании вновь выделяется углекислый газ, при этом красная окраска исчезает: H 2СO3 = СO2 + Н2О
Слайд 63Химические свойства оксида кремния (IV) и оксидов углерода (IV)
Оба оксида – типичные кислотные оксиды. Оксиды взаимодействуют с основными оксидами, щелочами. Оксид углерода (IV) при пропускании через раствор СO2 + 2NaOH t˚→ Na2 СO3 + H2O Оксид кремния (IV) при сплавлении 1) С основными оксидами: SiO2 + CaO t˚→ CaSiO3 2) Со щелочами: SiO2 + 2NaOH t˚→ Na2SiO3 + H2O
Слайд 64Химические свойства оксида углерода (II)
При обычных условиях CO инертен; при нагревании – восстановитель.
C+2O + CuO t˚C → Сu + C+4O2↑
На воздухе он горит голубым пламенем. При этом образуется углекислый газ.
1) Реакция с кислородом 2C+2O + O2 t˚C → 2C+4O2↑
2. Способен восстанавливать металлы из их оксидов. Именно это свойство используется в металлургии при выплавке чугуна.
3. Будучи несолеобраз.ующим оксидом, СО однако реагирует с расплавами щелочей с образованием солеподобного орг соединения- формиата, которое можно считать солью муравьиной кислоты
C+2O + NaOH P → HC+2OONa (формиат натрия)
Слайд 65Задание 8.
С помощью химических превращений разделите смесь оксида кремния (IV), карбоната кальция и серебра, последовательно растворяя компоненты смеси. Опишите последовательность действий.
Слайд 66Для того, чтобы отделить карбонат кальция используйте подсказку из предыдущего задания, не забудьте, что углекислый газ после выделения необходимо снова превратить в карбонат кальция. Для того, чтобы это сделать, вспомните качественную реакцию на углекислый газ . Однако в данном случае легче использовать соль, находящуюся в фильтрате, и реакцией обмена вновь получить из нее карбонат кальция Запишите уравнения реакции.
Слайд 671.К смеси прильем раствор соляной кислоты: СаСO3 + 2 HCl = СO2 + Н2О + СаCl 2 2. К отфильтрованному раствору добавим карбонат натрия: Na2СO3 + СаCl 2 = СаСO3 + 2 NaCl Отделим вновь получившийся карбонат кальция.
Слайд 68В смеси на фильтре остались серебро и оксид кремния (IV) . Для того, чтобы их разделить необходимо растворить одно из этих веществ, например серебро, которое легко восстановить из раствора солей.
Слайд 69В смеси на фильтре остались серебро и оксид кремния (IV) . Добавим азотную кислоту. Серебро растворяется с образованием нитрата серебра. Теперь можно отделить оксид кремния (IV) фильтрованием. 4. Оставшийся раствор упарим и прокалим . 2 АgNO3 = 2 Аg+ 2 NO2 + O2 Мы выделили серебро.
Слайд 70ТЕСТ 1. Соединения углерода и кремния очень похожи по своим физическим свойствам . 1.Да 2.Нет
ТЕСТ3 . Угарный газ легко вступает в реакции при обычных условиях. 1. Нет 2. Да
ТЕСТ 2 . Углекислый газ растворим в воде 1. Нет 2. Да
ТЕСТ 4. Углекислый газ - это типичный кислотный оксид 1. Да 2. Нет
ТЕСТ 5. Углекислый газ тяжелый, поэтому его можно переливать из стакана как жидкость. 1. Да 2. Нет
ТЕСТ 6 . Углекислый газ окисляется кислородом. 1. Да 2. Нет
Слайд 71Нет Да Да Нет Да Нет
Слайд 72Часть 4
Угольная и кремниевая кислоты , их соли.
каолинит (основная часть глины)
Полевой шпат Кремниевый топор
Слайд 73Н2SiO3— твердое вещество, практически нерастворимо в воде, поэтому катионы водорода в воде практически не отщепляются. В связи с этим такое общее свойство кислот, как действие на индикаторы, Н2SiO3 не обнаруживает, она еще слабее угольной кислоты. Н2SiO3 — непрочная кислота и при нагревании постепенно разлагается. Н2SiO3 = SiО2 + Н2О. Н2СО3 — существует только в растворе: Н2СО3 = Н2О + СО2
Формулы угольной и кремниевой кислот. Н2СО3 — угольная кислота, Н2SiO3 — кремниевая кислота.
Слайд 74Химические свойства кислот
Угольная кислота – двухосновная кислота, диссоциирует слабо в две ступени: H2CO3 ↔ H+ + HCO3-(гидрокарбонат-ион) HCO3- ↔ H+ + CO32- (карбонат-ион)
индикатор - лакмус краснеет в водном растворе углекислого газа:
Кремниевая кислота не диссоциирует.
Слайд 75Соли угольной и кремниевой кислот.
Угольная кислота образует два ряда солей: Средние соли - карбонаты Na2СO3, (NH4)2CO3 Кислые соли - бикарбонаты, гидрокарбонаты NaHCO3 , Ca(HCO3)2
NaHCO3 – питьевая сода
Na2CO3 – сода, кальцинированная сода
В природе встречаются карбонаты кальция CaCO3 в виде: мел мрамор известняк
Слайд 76Cuликаты — это соли кремниевой кислоты H2SiO3 Среди них наиболее распространены алюмосиликаты (понятно, что эти силикаты содержат алюминий). К алюмосиликатам относятся гранит, различные виды глин, слюды.
Слайд 77Физические свойства карбонатов и силикатов: Все карбонаты и силикаты– твёрдые кристаллические вещества. Большинство из них в воде не растворяются. Гидрокарбонаты растворяются в воде. Большинство силикатов в воде нерастворимо.
Это вещество часто называют жидким стеклом.
К растворимая солям кремниевой кислоты относятся силикаты щелочных металлов, например, натрия Na2SiO3
Древние бусы из стекла
Стекло – хрупкий, прозрачный материал, способен размягчаться и при застывании принимает любую форму. Обычное оконное стекло — это силикат состава Na2O•СаО•6SiO2.
Окрашенные стёкла получают введением в шихту (смесь исходных материалов) различных оксидов.

Слайд 78Качественная реакция на карбонаты и растворимые силикаты.
Действие сильных кислот на силикаты и карбонаты–
Na2SiO3 + 2HCl → 2NaCl + H2SiO3↓ SiO3 -2+ 2H + → H2SiO3↓
Na2СO3 + 2HCl → 2NaCl + H2 О + СO2 СO3 -2+ 2H + → H2 О + СO2
К растворимая солям кремниевой кислоты относятся силикаты щелочных металлов, например, натрия Na2SiO3. Анион соли соединяется с ионами водорода кислоты – получается нерастворимая, слабая кремниевая кислота. Эту реакцию можно считать качественной на анион силиката.
Слайд 79Химические свойства солей угольной кислоты: 1) Вступают в реакции обмена с другими растворимыми солями Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl 2) Разложение гидрокарбонатов при нагревании NaHCO3 t˚C → Na2CO3 + H2O + CO2↑ 3) Разложение нерастворимых карбонатов при нагревании CaCO3 t˚C → CaO+ CO2↑
Химические свойства солей кремниевой кислоты.
Силикаты реагируют 1) с кислотами Na2SiO3+2Н2O+2СО2=H2SiO3+2NaHCO3. 2) с солями Na2SiO3+CaCl2=2NaCl+CaSiO3↓

Слайд 80Взаимопревращение карбонатов и гидрокарбонатов
При избытке углекислого газа в присутствии воды карбонаты могут превращаться в гидрокарбонаты. Так, если через известковую воду пропускать углекислый газ, то она сначала помутнеет из-за выпавшего в осадок нерастворимого в воде карбоната кальция, однако при дальнейшем пропускании углекислого газа помутнение исчезает в результате образования растворимого гидрокарбоната кальция.
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
Эта реакция приводит к образованию накипи на стенках котлов, труб парового отопления и домашних чайников, , а в природе в результате этой реакции формируются в пещерах свисающие вниз. Другой способ превращения гидрокарбоната в карбонат – добавление основания, при этом кислая соль превращается в среднюю.
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3↓ + 2 H2O
Слайд 81Задание 9.
Приведите уравнения реакций, описывающие общие и специфические химические свойства угольной и кремниевой кислот.
Слайд 82Для того, чтобы записать уравнения общих реакций для этих веществ, необходимо вспомнить ) общие свойства всех кислот Реакции с оксидами Реакцции с основаниями Реакции с металлами .
Слайд 831) Реакции общие с другими кислотами, Как кислоты эти вещества реагируют одинаково с основаниями. Н2CO3 + 2NaOH = Na2CO3 + 2Н2О Н2SiO3 + 2NaOH = Na2CO3 + 2Н2О Н2CO3 реагирует также с активными металлами и оксидами металлов, а кремниевая поскольку является твердым веществом – только с основаниями: Н2CO3 + Mg = MgCO3 + Н2 Н2CO3 + СаО = СаСO3 + Н2О
Слайд 84Специфические свойства этих кислот определяются тем фактом, что обе кислоты очень слабые, при этом кремниевая слабее угольной.
Слайд 85Специфические свойства. кремниевая кислота не диссоциирует, поэтому в растворе угольная кислота вытесняет кремниевую из ее солей, а при прокаливании происходит обратное явление. Na2SiO3+2Н2O+2СО2=H2SiO3+2NaHCO3. Na2CO3+ SiО2=Na2SiO3 + СО2. Первый процесс обусловлен тем, что кремниевая кислота более слабая, чем угольная. Силикаты, входящие в состав минералов, в природных условиях разрушаются под действием воды и оксида углерода (IV) - это процесс выветривания горных пород Второй же процесс объясняется меньшей летучестью оксида кремния (IV).
Слайд 86Задание 10.
Какой объем углекислого газа необходимо пропустить (н. у.) через раствор массой 80 г с массовой долей растворенного вещества гидроксида бария 5% для получения гидрокарбоната бария?
Слайд 87Для успешного решения необходимо вспомнить, что такое массовая доля растворенного вещества в растворе, и найти массу вещества участвующего в реакции.
Слайд 88гидроксида бария составляет 5% от общей массы раствора. Найдем его массу m(Ва(ОН)2) = 80•0,05 = 4 г
Слайд 89
Слайд 903. Рассчитаем объем газа: V(СО2) = 0,0468•22,4 = 1,05 л. Ответ. 1,05 л СО2.
Составим уравнение реакции: 2. Рассчитаем количества веществ исходных соединений, вступивших в реакцию: (Ва(ОН)2) = 4/171 = 0,0234 моль; По уравнению реакции количество углекислого газа в 2 раза больше: (СО2) = 2 (Ва(ОН)2) = 2•0,0234 = 0,0468 моль.
Слайд 91ТЕСТ 1. Все кислоты реагируют с растворимыми основаниями с образованием соли и воды. Да Нет
Тест 2 . Кремниевая кислота реагирует с растворами солей. 1. Да 2.Нет
Тест 3. Кремниевая кислота хорошо реагируют с любыми оксидами. Да Нет
ТЕСТ 4 . Гидрокарбонаты хорошо растворяются в воде. 1. Да 2. Нет
ТЕСТ 5 . Стекло- твердое вещество молекулярной кристаллической решеткой.. 1. Нет 2. Да
Слайд 92Ответы. Да Нет Нет Да Нет
Слайд 93Список литературы.
«Химия. 9 класс» П.А.Оржековский, Л.М. Мещеряковская, Л.С. Понтак АСТ . ОАО «Московские учебники» 2007 «Химия. 9 класс. Базовый уровень» В.В.Еремин, А. А. Дроздов, Н.Е.Кузьменко,В.В.Лунин, учебник для общеобразоват. учреждений М. : Дрофа, 2007.