Слайд 1НИТРОВАНИЕ ЦЕЛЛЮЛОЗЫ
http://prezentacija.biz
Слайд 2Нитрование целлюлозы смесями азотной и серной кислот
Нитрование целлюлозы смесями HNO3–H2SO4–H2O является основным промышленным способом получения НЦ. Изменение состава кислотных смесей и условий процесса позволяет в необходимых пределах регулировать качественные показатели получаемых НЦ. Требуемая степень этерификации в пределах от 11,0 до 13,9% азота достигается в основном изменением содержания воды в кислотной смеси от 6 до 21%. Физико-химические показатели НЦ в значительной степени определяются температурно-временными параметрами процесса.

Слайд 3Влияние состава кислотной смеси а) Соотношение азотной и серной кислот
Соотношение азотной и серной кислот в смеси (при постоянном содержании воды) влияет в основном на скорость процесса нитрования. Чем содержание Н2SO4 в нитрующей смеси, тем ↓ скорость процесса нитрования, тем больше количество образующихся сернокислых эфиров и тем степень деструкции НЦ. Поэтому в производственных условиях отношение H2SO4 : HNO3 в нитрующих смесях не превышает 3:1 (по массе), хотя с экономической точки зрения целесообразно максимально
увеличивать содержание серной кислоты, т.к. ее стоимость ниже стоимости азотной кислоты. При увеличении соотношения H2SO4 : HNO3 повышается растворимость НЦ одной и той же степени нитрации. Увеличение содержания азотной кислоты улучшает смачивающие свойства кислотной смеси, что способствует повышению диффузии кислот внутрь волокон и приближает протекание процесса к кинетической области.

Слайд 4б) Содержание воды
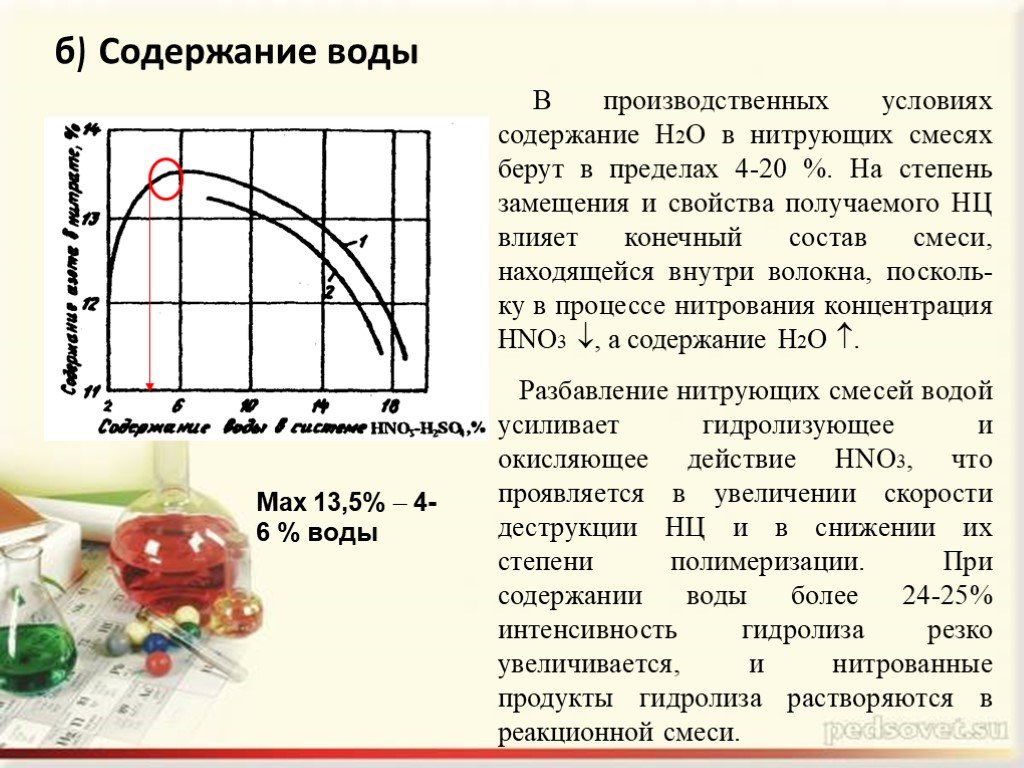
В производственных условиях содержание Н2О в нитрующих смесях берут в пределах 4-20 %. На степень замещения и свойства получаемого НЦ влияет конечный состав смеси, находящейся внутри волокна, посколь-ку в процессе нитрования концентрация HNO3 , а содержание Н2О . Разбавление нитрующих смесей водой усиливает гидролизующее и окисляющее действие HNO3, что проявляется в увеличении скорости деструкции НЦ и в снижении их степени полимеризации. При содержании воды более 24-25% интенсивность гидролиза резко увеличивается, и нитрованные продукты гидролиза растворяются в реакционной смеси.
Max 13,5% 4-6 % воды
Слайд 5Диаграмма состояния нитрующей системы
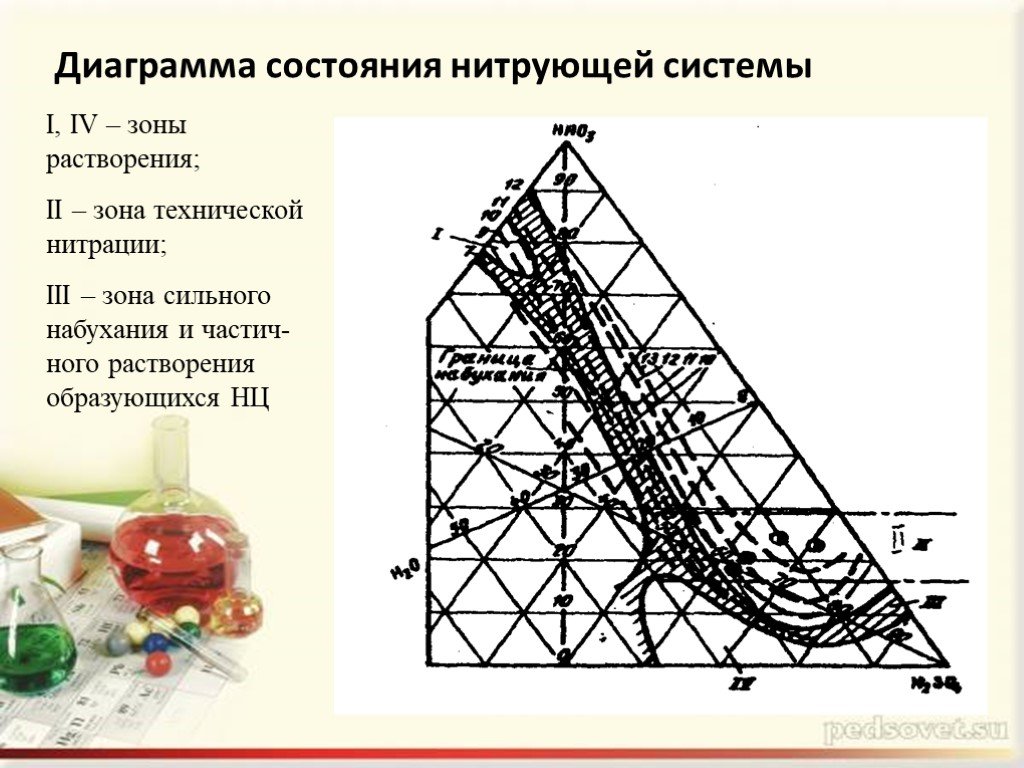
I, IV – зоны растворения; II – зона технической нитрации; III – зона сильного набухания и частич-ного растворения образующихся НЦ
Слайд 6в) Наличие оксидов азота в нитрующих смесях
Наличие оксидов азота в нитрующих смесях вызывает протекание реакций окисления и гидролиза целлюлозы, что приводит к понижению выхода НЦ, их вязкости и стабильности. Содержание оксидов азота в нитрующих смесях в заводских условиях допускается не более 4,5 %. Отрицательное действие оксидов азота особенно проявляется в кислотных смесях с повышенным содержанием воды (10 % и более). В маловодных нитрующих смесях подавляющая часть оксидов азота связывается серной кислотой и находится в виде нитрозилсерной кислоты:
N2O4 + H2SO4 HNO3 + NOHSO4 N2O3 + 2H2SO4 2NOHSO4 + H2O. Поэтому их гидролизующее и окисляющее действие проявляется в меньшей степени.

Слайд 7Влияние модуля ванны
Модулем ванны называют отношение массы нитрующей смеси к массе нитруемой целлюлозы. При получении НЦ применяется значительный избыток нитрующей сме-си. Это обусловлено малой величиной насыпной массы целлюлозы, гетеро-генностью и экзотермичностью процесса, разбавлением кислотной смеси выделяющейся при реакции водой. С увеличением модуля улучшается одно-родность получаемого НЦ по содержанию азота и физико-химическим показателям, вследствие лучшей смачиваемости исключается резкое измене-ние состава кислотной смеси и местные перегревы.
Чем больше модуль ванны, тем меньше повышается содержание воды в нитрующей смеси после нитрования и тем выше степень этерификации получаемого НЦ. При нитровании целлюлозы в заводских условиях величина модуля ванны зависит от вида целлюлозного материала и составляет для целлюлозы марки РБ 25-28, ЦА 33-38, ХЦ 40-45. Применение модулей больше указанных нецелесообразно экономически.

Слайд 8Влияние температуры
Температура нитрования влияет на скорость этерификации. С температуры скорости как основной реакции, так и побочных процессов окисления и гидролиза Ц и её нитратов. Поэтому с температуры степень полимеризации (вязкость растворов) НЦ , а их растворимость . В производстве это используется для регулирования вязкости НЦ. В заводских условиях температура реакции при получении высокоазотных НЦ составляет 25-30°С, а низкоазотных (низковязких) – 35-40°С.
Влияние продолжительности нитрования
Продолжительность нитрования Ц определяется временем, необходимым для диффузионного выравнивания концентрации нитрующей смеси внутри волокна и вне его. содержания HNO3 в нитрующей смеси, смачиваемости Ц и температуры способствуют поверхностного натяжения нитрующей смеси и скорости процесса нитрования. Нитрование рыхлого материала протекает очень быстро и заканчивается в течение нескольких минут. В производственных условиях для получения однородного продукта нитрование проводят в течение 30-90 мин. С увеличением времени нитрования вследствие протекания побочной реакции гидролиза понижается степень полимеризации НЦ, что также используется в практике для регулирования вязкости получаемого продукта.

Слайд 9Влияние свойств исходной целлюлозы
На диффузионные процессы и протекание собственно этерификации Ц большое влияние оказывают степень ее очистки от нецеллюлозных примесей (лигнина, смол, жиров) и форма Ц-ого материала. Примеси ухудшают смачиваемость Ц, замедляют процессы диффузии кислот внутрь волокна, затрудняют отжим отработанных кислот от нитратов и, в конечном итоге, понижают выход НЦ и его качественные показатели. ХЦ содержит значительно меньше примесей, чем древесная Ц, имеет более сохранившуюся капиллярную структуру, меньшую плотность, поэтому она легко впитывает кислотную смесь и хорошо смачивается при нитровании. НЦ на основе ХЦ лучше сохраняют капиллярную структуру, чем НЦ из древесных целлюлоз, поэтому процессы последующей переработки их протекают значительно легче. Повышение плотности исходной Ц и содержание в ней гидрофобных примесей затрудняют процессы капиллярной пропитки и диффузии и соответственно весь процесс нитрования. При нитровании целлюлозного материала с большей плотностью и меньшей гидрофильностью из-за наличия примесей необходимо увеличивать смачивающую способность кислотной смеси. Обычно это достигается повышением в ней содержания азотной кислоты и уменьшением содержания воды.

Слайд 10Механизм нитрования целлюлозы
Нитрование Ц представляет собой ряд накладывающихся друг на друга физико-химических и химических процессов: смачивание, капиллярная и межмолекулярная пропитка целлюлозного волокна нитрующей смесью, набухание целлюлозы в нитрующей смеси, собственно этерификация целлюлозы и диффузионное выравнивание состава нитрующей смеси внутри волокна за счет нитрующей смеси, окружающей волокно. Наряду с перечисленными процессами протекают побочные реакции: гидролиз и окисление целлюлозы, денитрация и деструкция НЦ. Степень превращения и скорость процессов, свойства получаемых НЦ зависят от химической природы Ц (разной реакционной способности первичных и вторичных гидроксильных групп, их доступности, наличия других функциональных групп – карбонильных, карбоксильных, остатков других полисахаридов), от макроскопических факторов (удельной поверхности целлюлозы, её смачиваемости нитрующей смесью, физической формы целлюлозного волокна, его структурной однородности) и особенно от свойств нитрующей смеси. При прочих равных условиях состав и строение получаемых НЦ определяются в первую очередь процессом взаимодействия Ц и нитрующей смеси.

Слайд 11Теоретические представления о механизме нитрования целлюлозы
Правило Д.И.Менделеева (1895 г.): в серно-азотных нитрационных смесях, применяемых для получения пироколлодийного пироксилина, «число водородных атомов воды должно равняться сумме атомов водорода азотной и серной кислот», т.е. должно соблюдаться соотношение: 2HNO3 + xH2SO4 + (x+1)H2O. А.В.Сапожников впервые рассмотрел процесс взаимодействия целлюлозы и нитрующей смеси как типично гетерогенную реакцию. Он предложил гидратную теорию нитрования Ц, сущность основных положений которой может быть сформулирована следующим образом:
Нитрующей способностью в кислотной смеси обладает только свободная азотная кислота в виде моногидрата (HNO3). Серная кислота выполняет роль водоотнима-ющего средства. max упругостью пара и соответ-но max нитрующей способностью обладает кислотная смесь состава HNO3 + H2SO4 + H2O, в которой вся HNO3 находится в свободном виде, а серная кислота в виде гидрата H2SO4 ·H2O.

Слайд 123. С повышением содержания воды в системе упругость паров и, соответственно, нитрующая активность смеси понижается, и при соотношении, когда вся серная кислота находится в виде дигидрата H2SO4·2H2O, а азотная в виде гидрата HNO3·H2O, нитрующее действие кислотной смеси прекращается. 4. В тройной кислотной смеси серная кислота связывает воду, превращаясь в гидраты H2SO4·H2O и H2SO4·2H2O; азотная кислота остается в негидратиро-ванном состоянии. Когда воды в смеси не хватает на превращение всей серной кислоты в гидрат H2SO4·H2O, негидратированная H2SO4 отщепляет воду от азотной кислоты с образованием азотного ангидрида: 2HNO3 + nH2SO4 → N2O5 + H2SO4·H2O + (n-1)H2SO4 Количество реакционноспособной азотной кислоты при этом уменьшается, и этим обусловлена худшая нитрующая способность безводной смеси HNO3 + H2SO4 по сравнению со смесями, содержащими 4-5 % воды. Последнее заключение является сомнительным, поскольку известно, что азотный ангидрид обладает высокой нитрующей способностью, и его наличие в смеси не должно приводить к снижению её реакционной способности. Теория нитросмесей Сапожникова в своё время сыграла большую роль. Было показано значение отдельных компонентов нитрационных смесей и намечены пути для правильного подбора их состава. Впервые дано объяснение роли серной кислоты и воды в составе нитрационных смесей.

Слайд 133. Ганч и Фармер (1925 г.) для объяснения закономерностей, наблюдаемых при нитровании Ц азотной кислотой и её смесями с серной кислотой, воспользовались представлениями об амфотерности HNO3. Согласно теории Ганча азотная кислота является амфотерным соединением и может существовать в виде двух форм: кислотной (аци-) HNO3 и псевдоформы Эфиры азотной кислоты построены по типу псевдоформы. Для безводной азотной кислоты также характерна псевдоформа. В присутствии воды или слабых кислот азотная кислота реагирует в ациформе (отдает протон, образуя нитрат оксония, например, с водой нитрат гидроксония): HNO3 + H2O H3O· NO3 В присутствии сильных кислот (например, серной) азотная кислота реагирует как основание с образованием нитрацидий-бисульфата:
HNO3 + H2SO4 H2NO3·HSO4 В безводной азотной кислоте возможно взаимодействие её аци- и псевдоформы с образованием нитрацидий-нитрата: HNO3 + HNO3 H2NO3· NO3

Слайд 14На основании представлений Ганча Фармер дал теоретическое обоснование закономерностям, наблюдаемым при нитровании целлюлозы. Основные положения его теории заключаются в следующем: 1. Нитрующим реагентом в кислотной смеси является псевдоформа азотной кислоты, и нитрующая способность кислотной смеси и степень нитрации получаемых НЦ зависят от её содержания в нитрующей смеси. 2. Максимальной нитрующей способностью обладает кислотная смесь состава HNO3 + H2SO4 +H2O, в которой вся азотная кислота находится в виде псевдоформы, а серная кислота в виде гидроксоний-бисульфата (H3O·HSO4). 3. По мере разбавления кислотной смеси водой последняя связывается азотной и серной кислотами, и нитрование прекращается при соотношении компонентов HNO3+H2SO4 +3H2O, когда вся серная кислота находится в виде гидроксоний-сульфата (H3O)2SO4, а азотная в виде гидроксоний-нитрата H3O·NO3.
4. При недостатке воды в смеси до образования H3O·HSO4 серная кислота взаимодействует с азотной кислотой с образованием нитрацидий-бисульфата H2NO3·HSO4, что приводит к уменьшению содержания псевдоформы и, соответственно, активности кислотной смеси. 5. В маловодной азотной кислоте при содержании воды менее 5% возможно образование нитрацидий-нитрата, что приводит к понижению её нитрующей способностью.

Слайд 15В последующих гипотезах о механизме реакций нитрования спиртов Ингольда и Еременко использованы современные данные о строении и свойствах компонентов реагирующих систем. Как известно, наличие подвижного протона и неподеленной пары электронов на кислородном атоме гидроксильной группы молекулы азотной кислоты обуславливает её способность участвовать в реакциях, принимая и отдавая протон. В более основных, по сравнению с азотной кислотой, средах последняя выступает в качестве донора протона с образованием оксониевого иона и нитрат-аниона. Например, в водных растворах реакция протекает по схеме: HNO3+H2O H3O++NO3- При этом процесс ионизации HNO3 протекает через промежуточную стадию образования сольватов (гидратов): HNO3 + nH2O HNO3·nH2O В итоге водный раствор азотной кислоты характеризуется наличием частиц HNO3, HNO3·nH2O, NO3-, H2O. При высоких концентрациях (вплоть до 100 %) проявляются амфотерные свойства HNO3 и в составе появляются продукты равновесных реакций её автопротолиза: HNO3 + HNO3 H2NO3+ + NO3- H2NO3+ NO2+ + H2O NO2+ + NO3- N2O5 100 %-ная азотная кислота содержит около 97 % молекул HNO3, 1,0 % NO2+, 1,5 % NO3-, 0,5 % H2O и незначительное количество N2O5.

Слайд 16Если в качестве растворителя используются более сильные кислоты, чем азотная кислота (например, серная), реакции кислотно-основного равновесия с образованием нитроний-катиона протекают на большую глубину: HNO3 + 2H2SO4 NO2+ + 2HSO4- + H3O+
3. Ингольд и его коллеги (1958 г.) механизм нитрования спиртов полагали подобным О-нитрованию. В своей теории они основывались на результатах предшествующих работ Клейна и Ментсера (1951). При нитровании целлюлозы азотной кислотой происходит замещение протона гидроксильной группы на NO2 –группу, а не ОН на NO3: R O H + HO NO2 → RONO2 + H2O
Согласно представлениям Ингольда нитрующим агентом при О-нитровании спиртов является катион нитрония NO2+. Его образование в растворах азотной кислоты протекает по схеме: HNO3 + HNO3 H2NO3+ + NO3- (быстро) H2NO3+ NO2+ + H2O (медленно) Процесс идет в две стадии: 1) присоединение иона нитрония 2) отрыв протона NO2 NO2 ROH + NO2+ RO H + RO H ++NO3-→RONO2+ HNO3 (быстро) (быстро)
k1 k2 k2

Слайд 17Роль H2SO4 заключается в том, что она участвует в протонизации HNO3: HNO3 + H2SO4 HSO4- + H2NO3+, а также связывает воду, способствуя повышению концентрации нитроний-катиона: H2SO4 + H2O HSO4- + H3O+
4. Еременко (1960 г.) при нитровании многоатомных спиртов наблюдал образование нитратов в такой области концентраций, когда HNO3 находилась в неионизированном состоянии (т.е. в ней отсутствовали катионы нитрония). В то же время анализ кислотных смесей, используемых в промышленных условиях для получения НЦ, показал, что наличие в их составе заметных количеств NO2+ маловероятно (Рис.).
Это указывает на возможность существования в серноазотных кислотных смесях иных
нитрующих агентов. Еременко обратил внимание на то, что спирты обладают основными свойствами и в нитрующих смесях ионизируются с образованием соответствующих протонированных форм. Он предположил, что нитруется протонированная форма спирта ROН2+.

Слайд 18Основные положения гипотезы Еременко: 1. Нитрующим агентом является свободная неионизированная молекула HNO3. 2. Образование нитроэфиров протекает по следующему механизму: а) протонизация спирта азотной кислотой с образованием оксониевого иона ROH + HONO2 ROН2+ + NO3- (быстро), б) образование комплексного соединения ROН2+ + HNO3 [ROН2 ·HONO2]+ (медленно), в) распад промежуточного комплекса с образованием нитроэфира Н [ROН2 ·HONO2]+ RO+ NO2 + Н2О (медленно), Н RO+ NO2 + NO3- RONO2 + HNO3 (быстро). Серная кислота участвует в реакции протонирования спирта: ROH + H2SO4 ROН2+ + HSO4-, а также связывает воду: H2SO4 + H2O HSO4- + H3O+ Отмечается возможность образования нитроэфиров в азотнокислых средах через взаимодействие протонированного спирта с пентоксидом диазота (N2O5): Н ROН2+ + N2O5 → RO+ NO2 + HNO3 Пентоксид диазота образуется в небольших количествах в растворах азотной кислоты по реакции: NO2+ + NO3- N2O5
Слайд 19