Презентация "Амины" по химии – проект, доклад
Презентацию на тему "Амины" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 19 слайд(ов).
Слайды презентации
Список похожих презентаций
Органическая химия. Амины
Содержание : - Введение - Номенклатура - Химические свойства - Применение - Получение - Некоторые наиболее известные амины - Вредное воздействие. ...Амины и анилин
Решите задачу. Органическое вещество содержит 38,7% углерода, 45,15% азота и 16,15% водорода. Относительная плотность его паров по водороду равна ...Амины урок
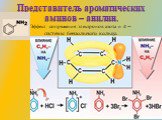
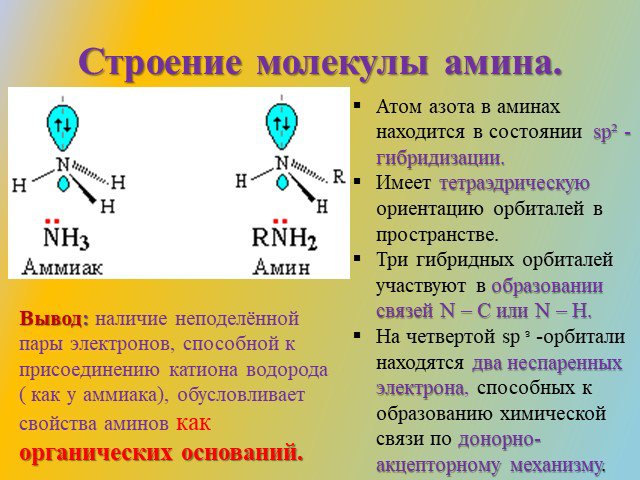
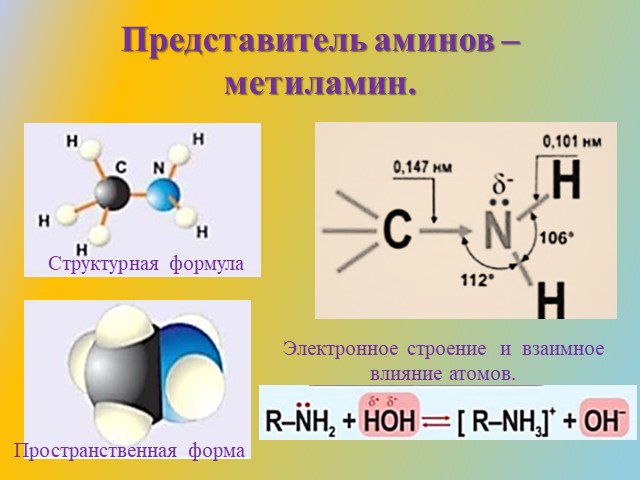
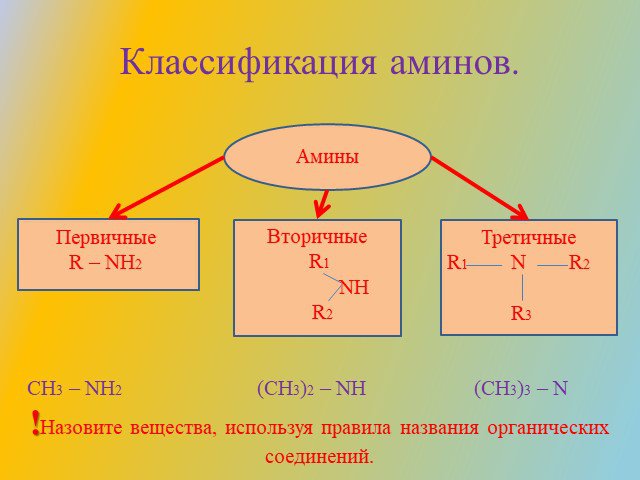
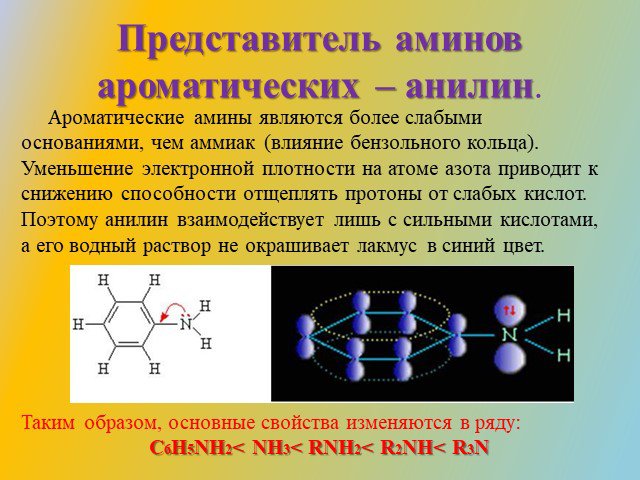
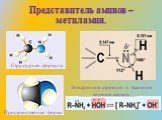
Классификация аминов. Первичные амины. -NH2 аминогруппа СН3-NH2 метиламин С6Н5-NH2 фениламин (анилин). Амины - органические основания. .. .. H : N ...Амины (органические производные аммиака)
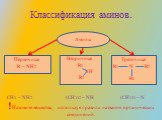
Амины (органические производные аммиака). Классификация. Первичные RNH2 ArNH2 Вторичные R-NH-R’ Ar-NH-R Третичные. Номенклатура. . Получение. Восстановление. ...Амины
Ами́ны — органические соединения, являющиеся производными аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные ...Амины
Назовите вещества. а) С3Н8 б)С2Н 4 в) С2Н2 г)С2Н5ОН д)СН3СНО е) СН3СООН ж) СН3NH2 з ) C2H5NH2. Амины. Что хочу узнать? Номенклатура аминов Физические ...Амины
Цели урока. Знать строение предельных алифатических аминов Уметь объяснять зависимость свойств органических соединений от их строения на примере аминов ...Амины
. . . . . . C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O 1842г. Н.Н. Зинин 13.08.1812 06.02.1880. Альма-матер: Казанский университет. Август Вильгельм ...Химия амины
Цели урока. Дать понятие об аминах, их классификации, изомерии, номенклатуре и свойствах в сравнении с аммиаком. Рассмотреть способы получения аминов. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:16 апреля 2015
Категория:Химия
Автор презентации:Г. П. Яценко, учитель химии
Содержит:19 слайд(ов)
Поделись с друзьями:
Скачать презентацию








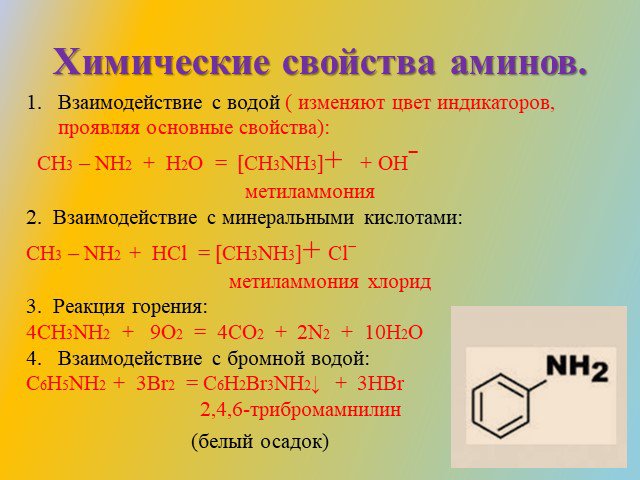











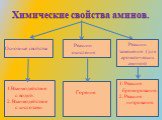
![Взаимодействие с водой ( изменяют цвет индикаторов, проявляя основные свойства): CH3 – NH2 + H2O = [CH3NH3]+ + OHˉ метиламмония 2. Взаимодействие с минеральными кислотами: CH3 – NH2 + HCl = [CH3NH3]+ Clˉ метиламмония хлорид 3. Реакция горения: 4CH3NH2 + 9O2 = 4CO2 + 2N2 + 10H2O Взаимодействие с бром Взаимодействие с водой ( изменяют цвет индикаторов, проявляя основные свойства): CH3 – NH2 + H2O = [CH3NH3]+ + OHˉ метиламмония 2. Взаимодействие с минеральными кислотами: CH3 – NH2 + HCl = [CH3NH3]+ Clˉ метиламмония хлорид 3. Реакция горения: 4CH3NH2 + 9O2 = 4CO2 + 2N2 + 10H2O Взаимодействие с бром](https://prezentacii.org/upload/cloud/15/04/24483/images/thumbs/screen13.jpg)