Презентация "Химия «Гидролиз солей»" – проект, доклад
Презентацию на тему "Химия «Гидролиз солей»" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 24 слайд(ов).
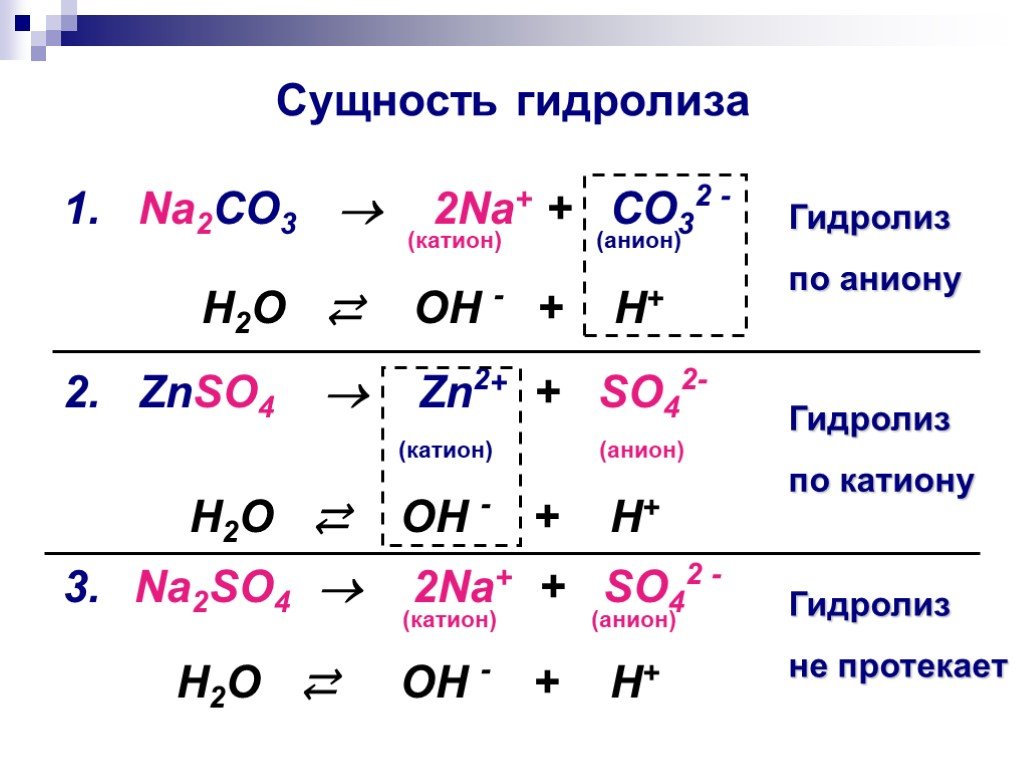
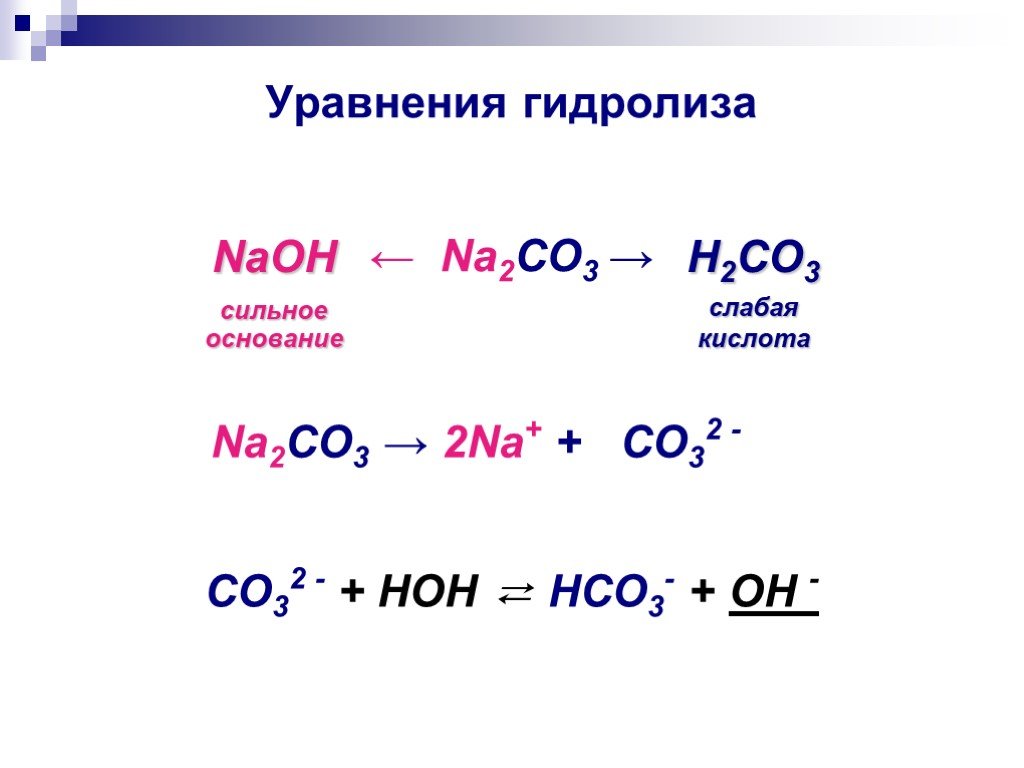
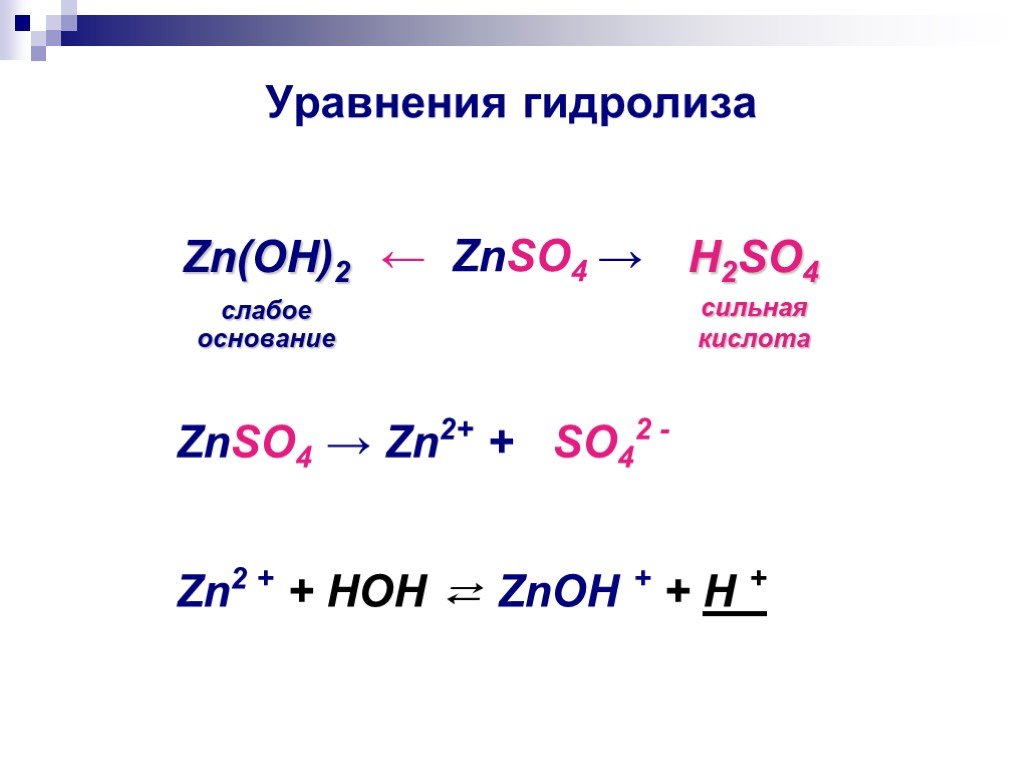
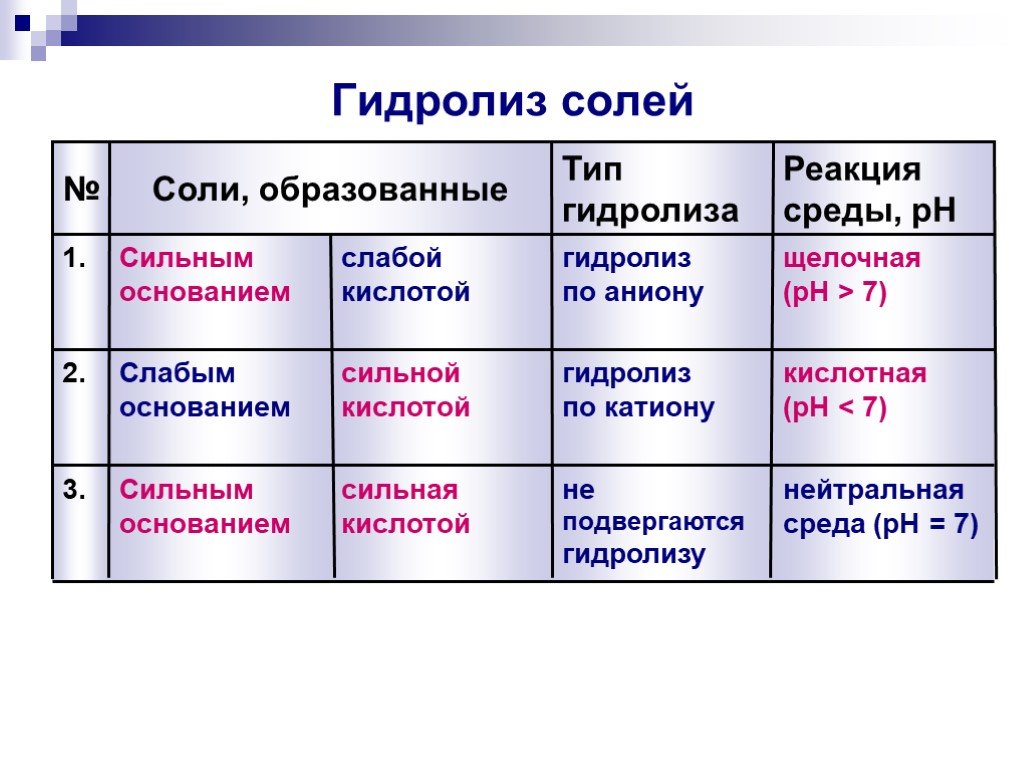
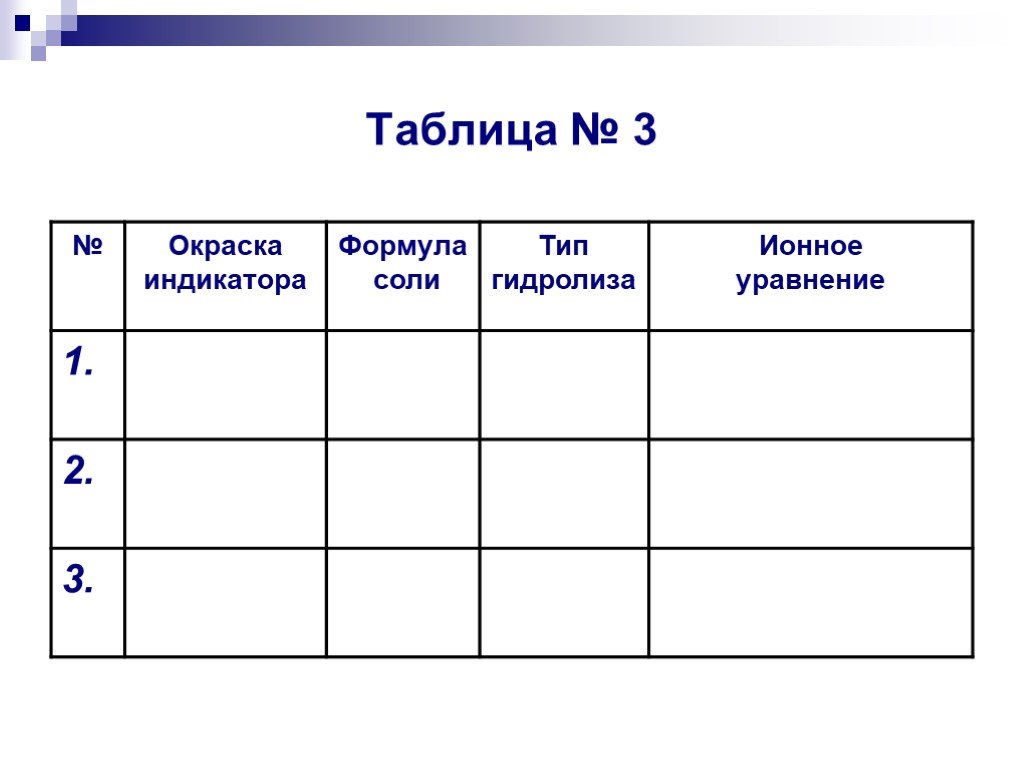
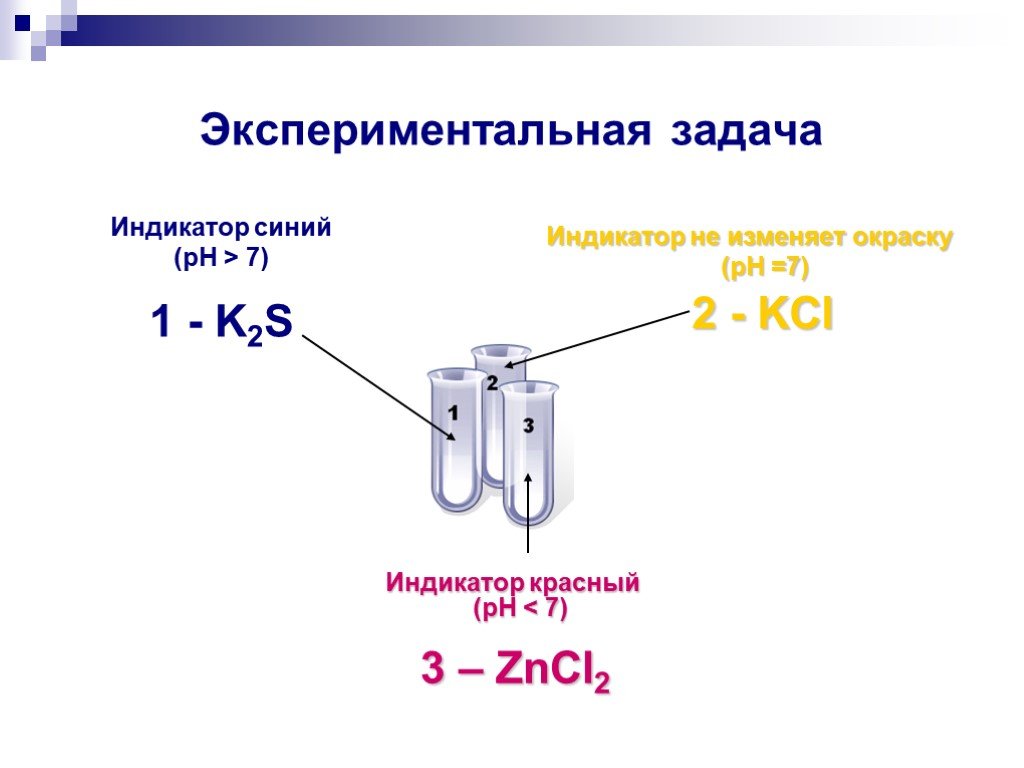
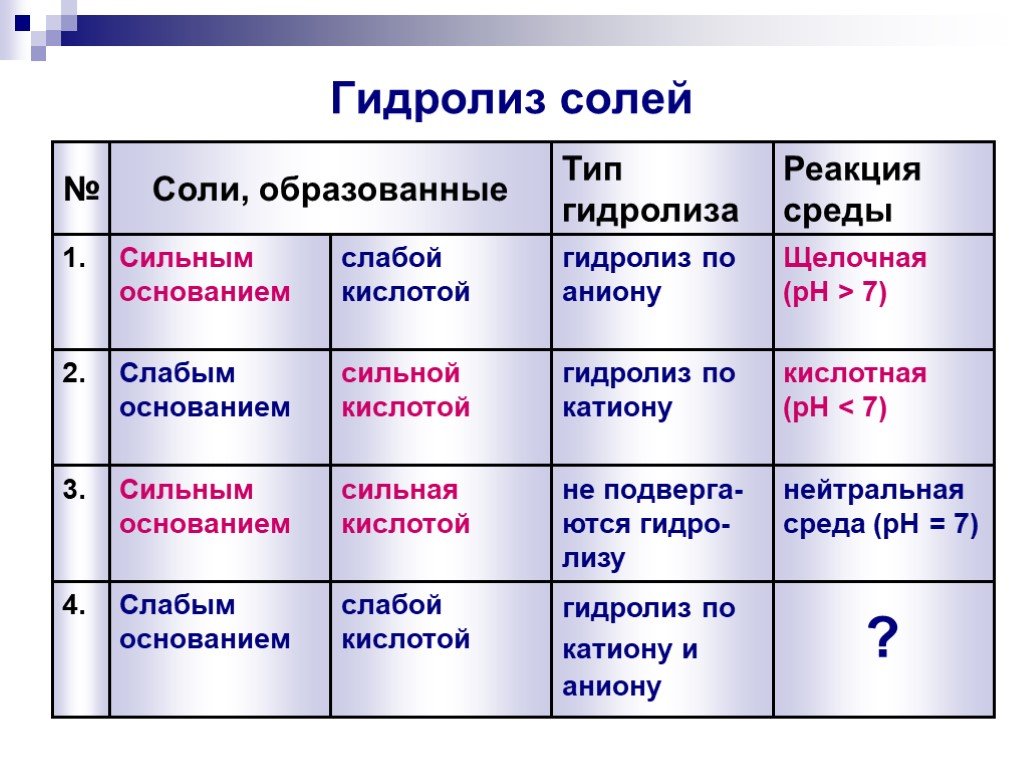
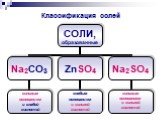
Слайды презентации
Список похожих презентаций
Химия Предельные углеводороды
1.Строение предельных углеводородов. 2.Гомологический ряд метана. 3.Таблица 1 гомологический ряд алканов. 4.Изомерия и номенклатура. 5.Получение. ...Путешествие по континенту Химия
Мотивация. Уважаемые участники! Вы начали изучать интересную и сложную науку химия. Химии принадлежит ключевая роль в ряду других наук (математика, ...Химия и эволюция
Особенности химии. Физика вырабатывает фундаментальные концепции и модели естествознания. Особенность химии состоит в том, что экспериментальное моделирование ...Химия мыла
Исследуемое мыло. «Чистая линия» «Невское» «DURU» «Молочное» «Детское мыло» «Дивный сад» «Palmolive». Физические свойства. Вредные вещества. Триэтаноламин ...Химия и повседневная жизнь человека
Узнать где и как в повседневной жизни человека используется химия. Гипотеза. Каждый день мы совершаем обычные на первый взгляд действия: солим еду, ...Химия и производство. Химическая промышленность и химическая технология
Химическая промышленность. - это отрасль народного хозяйства, производящая продукцию на основе химической переработки сырья. Основой химической промышленности ...Химия - решение задач
В этой презентации представлены материалы из пособия по химии «Решение расчетных задач школьного курса химии 8-11 классов». Решение задач 1-го типа ...Химия и наркотические вещества
Спирт как универсальный растворитель, или К чему ведет выпивка? 2. Перегонка табака, или Что мы курим? 3. Все наркотики убивают по-разному 4. Растворение ...Химия
Целью данных уроков является:. В занимательной форме повторить и обобщить материал базового курса химии; Научить применять полученые знания для решения ...Химия
ВУЗы, для поступления в которые нужно сдавать ЕГЭ по химии Медицинский университет Политехнический университет Сельскохозяйственная академия Педагогический ...Химия
СЛОВО О ПОЛЬЗЕ ХИМИИ, В ПУБЛИЧНОМ СОБРАНИИ ИМПЕРАТОРСКОЙ АКАДЕМИИ НАУК СЕНТЯБРЯ 6 ДНЯ 1751 ГОДА, ГОВОРЕННОЕ МИХАЙЛОМ ЛОМОНОСОВЫМ... ...Широко распростирает ...Химия
CO2 CH4 H2CO3 CuS C2H4 CH3OH C10H22 CaCO3 C2H5 OH. Какие вещества относятся к органическим. Чем отличаются органические вещества? Причины многообразия ...Путешествие по континенту Химия, познавательная игра по химии, 8 класс
“Наши знания не могут иметь конца именно потому, что предмет познания бесконечен” (Паскаль). Государство № 1 «Врата учёности». Ответ Be N Si Al P ...Химия и жизнь человека
Содержание. Химия и пища Химические средства гигиены и косметики Химические вещества в быту Химия и производство Химия и сельское хозяйство Химия ...Химия - страна чудес
- очень древняя наука. Выдающиеся русские химики. М.В. Ломоносов Д.И.Менделеев А.М.Бутлеров (1834-1907) (1711-1765) (1828-1886). химия физика медицина ...Химия и космос
Космос в популярном сознании представляется царством холода и пустоты. Однако примерно с середины XIX века исследователи стали понимать, что пространство ...Химия – наука о веществах, их свойствах и превращениях
Техника безопасности в кабинете химии. Вещества хранятся в емкостях с плотно притертыми пробками.. При проведении опытов строго соблюдайте инструкции ...Химия и пища
План. Вступление Пищевые добавки Классификация пищевых добавок Виды пищевых добавок Ароматизаторы Консерванты Витамины Эмульгаторы Антиокислители ...Химия – наука чудес и превращений
ХИМИЧЕСКИЙ ТУРНИР «Химия- наука чудес и превращений». Девиз: «Химии требуется не такой, который из одного чтения книг понял всю науку, но который ...Химия и проблемы охраны окружающей среды
В наши дни проблема охраны окружающей среды чрезвычайно возросла в связи со значительным, а очень часто и катастрофическим воздействием хозяйственной ...Конспекты
Химия как часть естествознания
7 класс. Естествознание. . Урок 1 Химия как часть естествознания. Предмет химии. Цель:. знакомство с понятиями тело, вещество, свойства веществ; ...Химия на досуге
Внеклассное мероприятие «Химия на досуге». Цель мероприятия: Развивать интерес к предмету химия, смекалку, эрудицию, умение чётко и быстро формулировать ...Химия и повседневная жизнь человека
Брусова Татьяна Викторовна. МБОУ « СудогодскаяСОШ №2» г. Судогда. Учитель химии. Урок по химии в 11 классе. . . Тема «Химия и повседневная ...Химия как наука
Муниципальное бюджетное общеобразовательное учреждение города Новосибирска. "Средняя общеобразовательная школа № 78". . Химия ...Химия и повседневная жизнь
Урок химии в 11 классе «Химия и повседневная жизнь». Учитель Зеленкина О.В. Цель: создать условия для изучения темы урока, понимания значения химических ...Химия и повседневная жизнь человека
Тема урока в 9 классе. Химия и повседневная жизнь человека. Цель урока:. Определить роль химической науки в современной жизни и доказать, что ...Химия и общество
Бюджетное образовательное учреждение г.Омска. . «Средняя общеобразовательная школа№15». Конспект урока по химии в 9 классе. «ХИМИЯ И ОБЩЕСТВО». ...Химия и кулинария
Методическая разработка внеклассного мероприятия. на тему: «Химия и кулинария». (Аукцион). Автор: учитель химии. . Бижоева Лариса Аскеровна. ...Химия в руках художника
. Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». г.Нижнекамск Республика Татарстан. Конспект интегрированного ...Химия в моей жизни
МАОУ СОШ № 170 г. Екатеринбурга. Химия в моей жизни. . . Программа элективного курса. . . . . Дубровина Елена Николаевна,. . ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:6 марта 2019
Категория:Химия
Содержит:24 слайд(ов)
Поделись с друзьями:
Скачать презентацию