Презентация "Кремний" (9 класс) по химии – проект, доклад
Презентацию на тему "Кремний" (9 класс) можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 24 слайд(ов).
Слайды презентации
Список похожих презентаций
Кремний и его соединения
Дать общую характеристику элементу кремний. Рассмотреть природные соединения кремния. Провести сравнительный анализ с соединениями углерода. Изучить ...Кремний
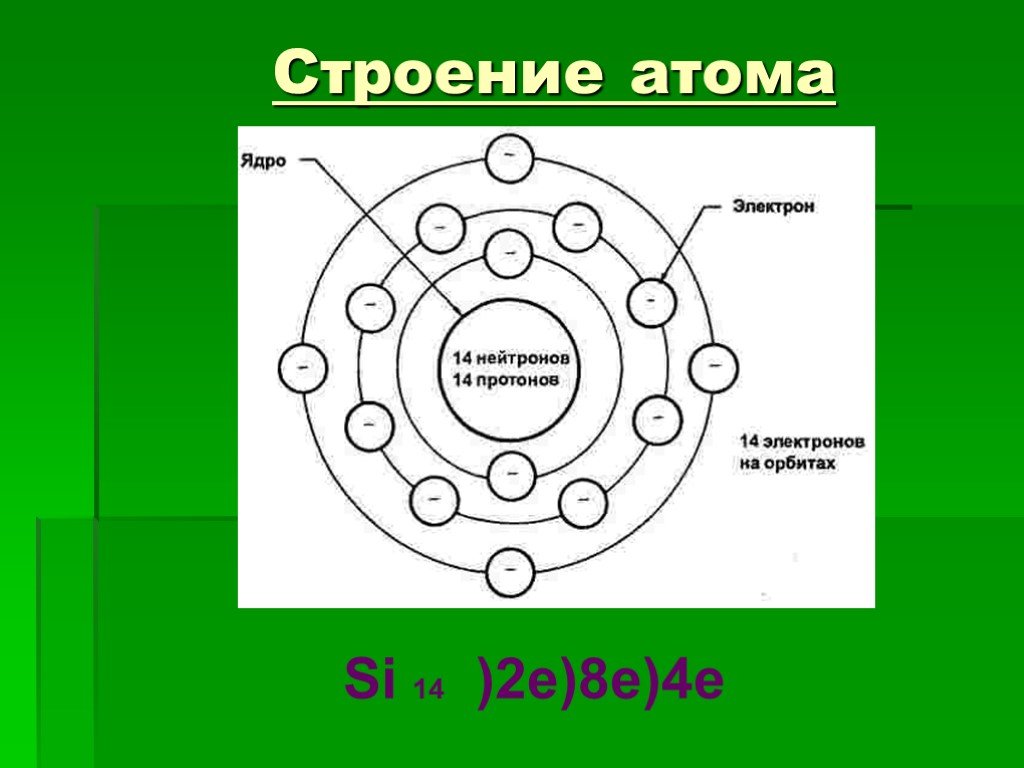
Общая характеристика кремния по положению в периодической системе. Порядковый номер – 14, заряд ядра +14, протонов в ядре – 14, электронов – 14. Номер ...Кремний, его физические и химические свойства
Цели урока: - рассмотреть положение кремния в периодической системе Д.И.Менделеева и строении его атома; - рассмотреть нахождение кремния в природе; ...Кремний и его соединения
Нахождение в природе. SiO2 кремнезём (песок). Al2O3∙ 2SiO2∙2H2O каолинит (глина). По распространенности занимает второе место после кислорода (26%). ...Кремний и его соединения
Короткова Фаина Алексеевна, учитель химии и биологии МБОУ Летуновской СОШ. Контактная информация: - e-mail: korotkova_faina@mail.ru - тел. +7 903 ...Кремний в природе
9 класс. КРЕМНИЙ В ПРИРОДЕ ИСПОЛЬЗОВАНИЕ КРЕМНЕЗЕМА ДЛЯ ПРОИЗВОДСТВА СТЕКЛА ПРИМЕНЕНИЕ СТЕКЛА. Si – ВТОРОЙ ПО РАСПРОСТРАНЕННОСТИ ЭЛЕМЕНТ НА ЗЕМНОМ ...Кремний
В главной подгруппе четвёртой группы В третьем малом периоде Возможные степени окисления: -4, 0, +2, +4. Si – ВТОРОЙ ПО РАСПРОСТРАНЕННОСТИ ЭЛЕМЕНТ ...Кремний
Si 30,9738 Р S 32,064 Сера 16 Cl 17 Al 13 Алюминий 26,982 I 10 Периоды Ряды.Периодическая система химических элементов Д.И.Менделеева.
39,948 24,312 ...
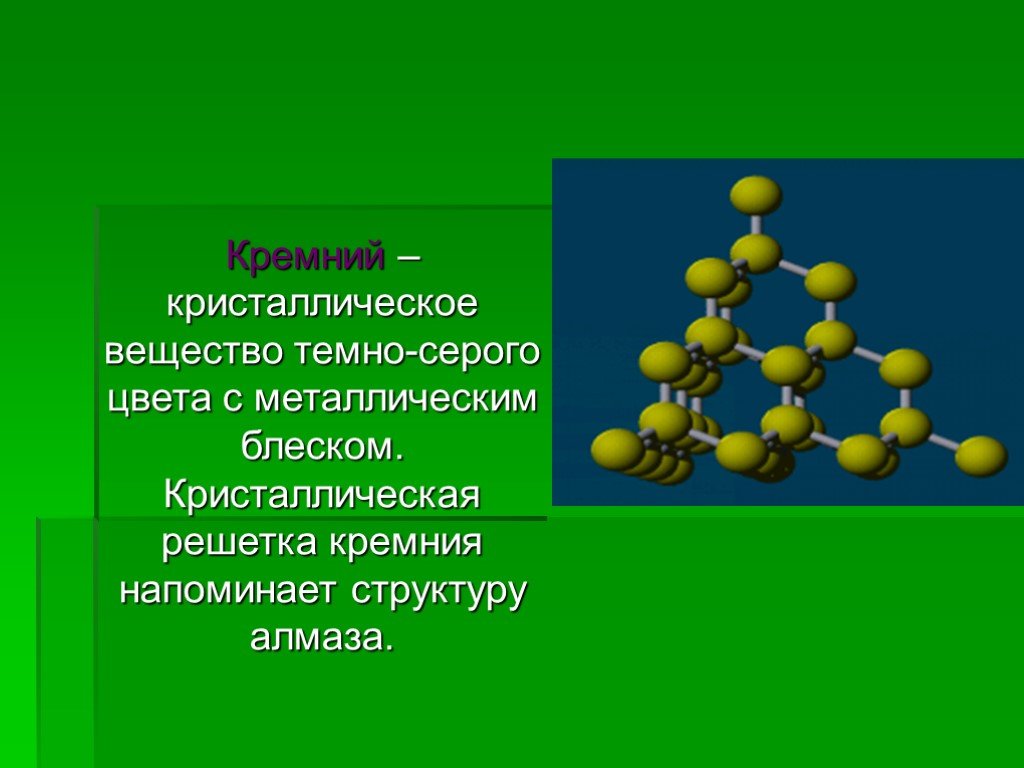
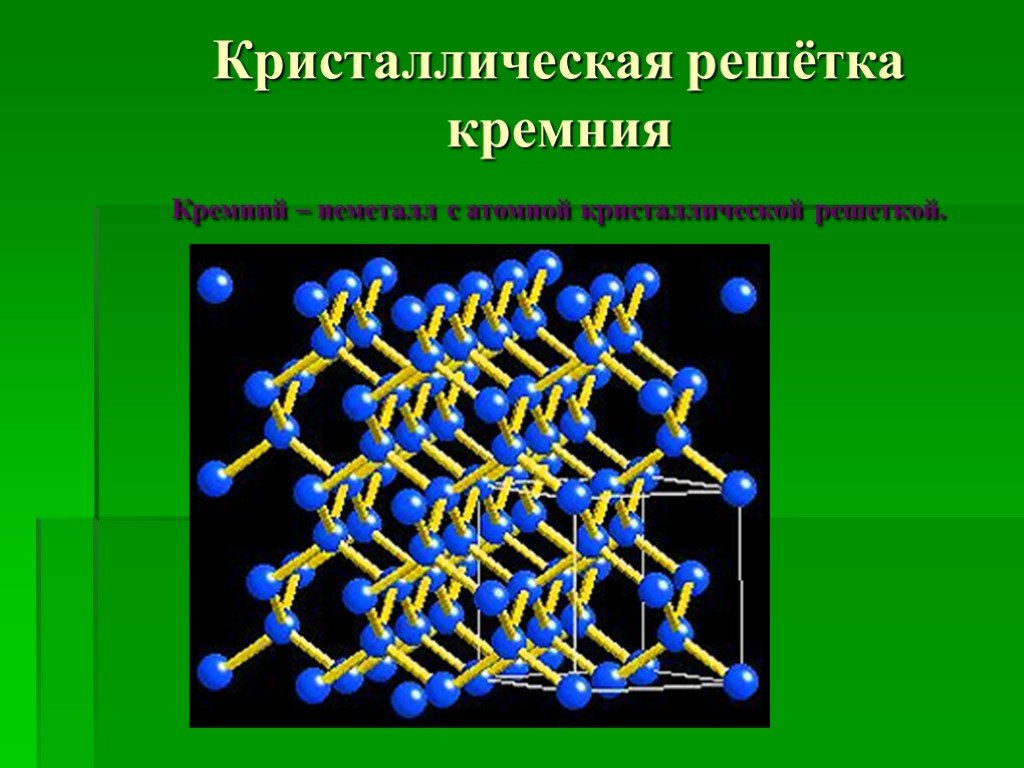
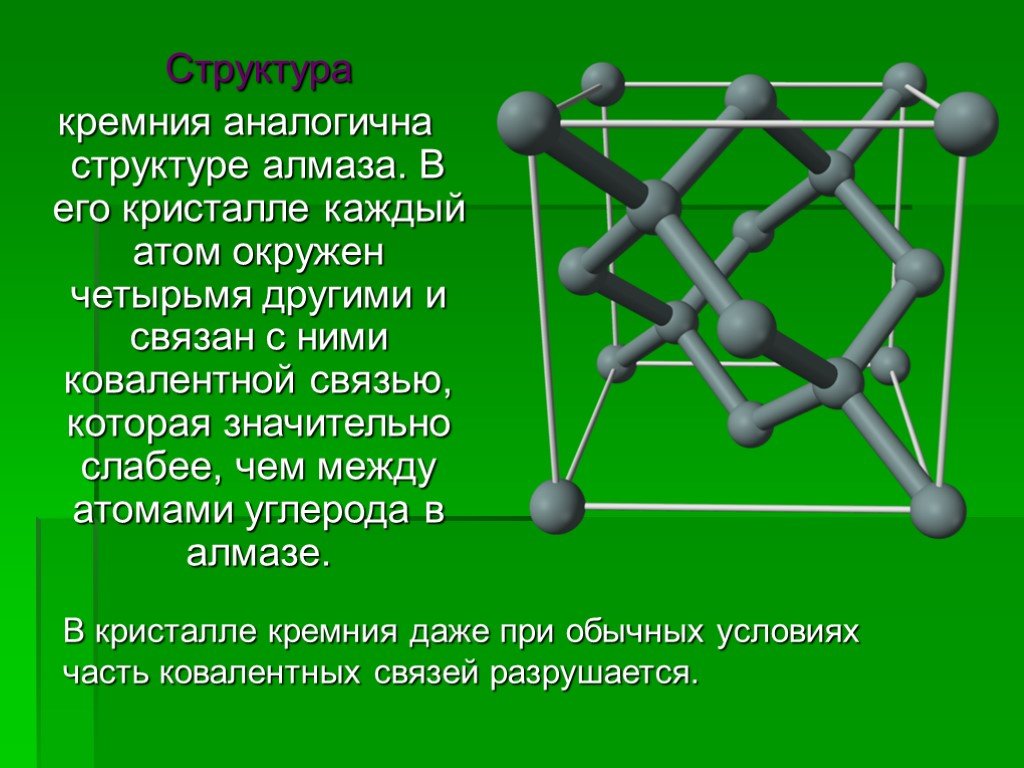
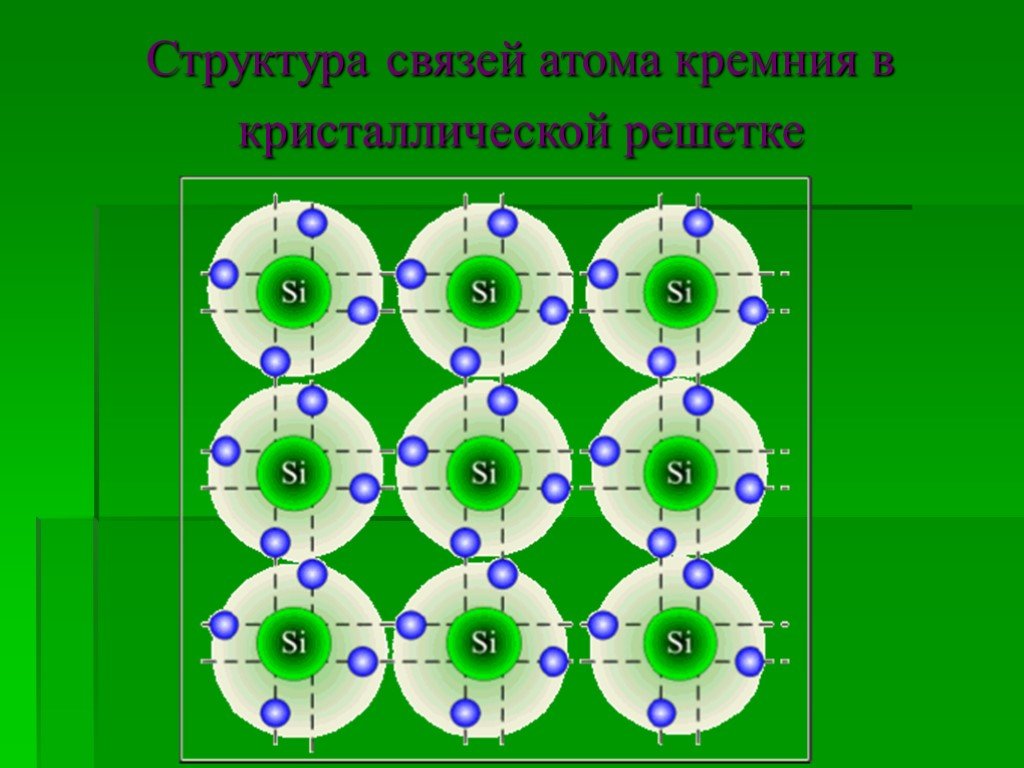
Кремний
Положение в ПСХЭ Д.И.Менделеева. ↑ ↑↓ 1s2 Строение атома 14Si 2e 4e 8e. № 14 Ar(Si) = 28 Z =+14, 14p+, 14e-, 14n0. р - элемент 28 2p6 2s2. В природе ...Интерактивная игра "Химия в ребусах: Химические элементы"
НИКЕЛЬ. ИОД. АЗОТ. БОР. МАГНИЙ Й. МАРГАНЕЦ. КРЕМНИЙ Л=й. МЫШЬЯК. УГЛЕРОД О. ЦИРКОНИЙ. АРГОН. МЕДЬ ДВЕ. КРИПТОН. ЗОЛОТО. СЕРА П=А. ВОДОРОД А=О Т=Д. ...«Электролитическая диссоциация» химия
Электролитическая диссоциация. H2O. Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией. ...«Окислительно-восстановительные реакции» химия
СОДЕРЖАНИЕ:. 1. Какие реакции называются окислительно-восстановительными? 2. Что называют окислителем, восстановителем? 3. Окислительно-восстановительный ...«Нуклеиновые кислоты» химия
Цель урока: сформировать у студентов понимание взаимосвязанности и взаимозависимости веществ в клетке. Задачи урока: повторить строение и основные ...«Задачи» химия
- исследование задач по нанонауке; - ознакомление с наномиром: о достижениях нанохимии и нанотехнологии; - составление задач по нанонауке; - решение ...«Жиры» химия
жиры. Оглавление. Определение и общая формула Физические свойства Химические свойства Классификация жиров Животные жиры Растительные жиры Роль жиров ..."Химические элементы и вещества"
Цель урока:. Повторить основные вопросы по изученному разделу “Вещества и химические явления”, закрепить полученные знания. Физические свойства веществ. ...Современная химия
Учение о составе вещества. Химический элемент - вид атомов с одинаковым зарядом ядра. Индивидуальность химического элемента обусловлена: зарядом ядра ...Предельные углеводороды химия
Органическая химия – это раздел химической науки, в котором изучаются соединения углерода и их превращения. В наши дни к органическим веществам относятся ...Сера химия
Сера принадлежит к числу веществ, известных человечеству испокон веков. Ещё древние греки и римляне нашли ей разнообразное практическое применение. ...Полезная химия во фруктах и овощах
1 3 4 5 6 7 8 9 10 11 13 14. Химический состав сока во многом схож у различных видов этих фруктов: сок плодов содержит: сахара, органические кислоты, ...Конспекты
Кремний и его соединения. Стекло. Цемент
Дата_____________ Класс_______________. Тема:. . Кремний и его соединения. Стекло. Цемент. Цели урока:. знать состав, строение, свойства оксидов ...Кремний и его соединения
Конспект урока химии «Кремний и его соединения». Приветствую тебя, мой юный исследователь! Предлагаю тебе сегодня обратиться самым настоящим пиратом. ...Кремний – химический элемент или природный дар. ...Силикаты
9 класс химия ( Габриелян). Учебное занятие № 44. Дата:. Тема: Кремний – химический элемент или природный дар. ...Силикаты. Эпиграф к уроку:. ...Кремний и его соединения
Т.В.Кузнецова,учитель химии, школа № 53. . ПЛАН-КОНСПЕКТ УРОКА. . «Кремний и его соединения». (тема урока). . ФИО Кузнецова Татьяна ...Кремний
Муниципальное бюджетное общеобразовательное учреждение. «Гимназия №32». г.Нижнекамск Республика Татарстан. Конспект урока по химии в 9 классе«. ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:5 сентября 2018
Категория:Химия
Классы:
Содержит:24 слайд(ов)
Поделись с друзьями:
Скачать презентацию






































![Силикаты. Силикаты – химические соединения, содержащие кремнекислотные остатки различного состава [SinOm]. Основа всех силикатов - кремнекислородный тетраэдр [SiO4], в центре которого расположен атом кремния, а в вершинах – атомы кислорода. Силикаты. Силикаты – химические соединения, содержащие кремнекислотные остатки различного состава [SinOm]. Основа всех силикатов - кремнекислородный тетраэдр [SiO4], в центре которого расположен атом кремния, а в вершинах – атомы кислорода.](https://prezentacii.org/upload/cloud/18/09/68053/images/thumbs/screen22.jpg)
































