Презентация "Электролиз" по химии – проект, доклад
Презентацию на тему "Электролиз" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 17 слайд(ов).
Слайды презентации
Список похожих презентаций
Электролиз .
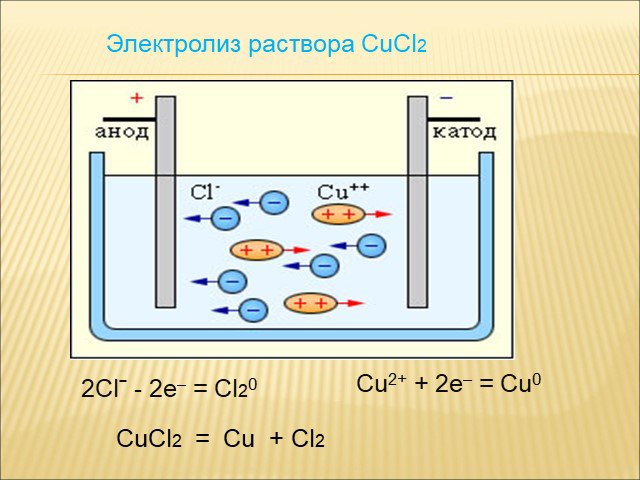
Электролиз – окислительно-восстановительный процесс, происходящий на электродах при пропускании постоянного электрического тока через раствор или ...Электролиз расплавов и растворов
Электролиз расплавов и растворов. Электролиз-это совокупность окислительно-восстановительных процессов,протекающих при прохождении постоянного электрического ...Электролиз
. Области применения электролиза. В основной химической промышленности – получение H2, O2, S, галогенов, щелочей и др. Электрометаллургия – получают ...Электролиз
Как наша прожила б планета? Как люди жили бы на ней Без теплоты, магнита, света И электрических лучей? Адам Мицкевич. Эпиграф урока. Проблемный вопрос. ...Электролиз
Терминология. Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, ...Электролиз
Определение:. Электро́лиз — физико-химическое явление, состоящее в выделении на электродах составных частей растворённых веществ или других веществ, ...Анод + Катод = Электролиз
Цель работы:. Изучить сущность процесса электролиза и выяснить области его применение. Содержание: Электролиз расплава Электролиз раствора Схема электролиза ...Конспекты
Химические реакции. Электролиз
ПЛАН-КОНСПЕКТ УРОКА Тема урока. : Электролиз. . ФИО. . . Хубиева Людмила Руслановна. . . . Место работы. . МБОУ СОШ ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:14 сентября 2014
Категория:Химия
Автор презентации:учитель Хайдарова Милявша Хуснулловна
Содержит:17 слайд(ов)
Поделись с друзьями:
Скачать презентацию