Презентация "Строение атомного ядра" по физике – проект, доклад
Презентацию на тему "Строение атомного ядра" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Физика. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 17 слайд(ов).
Слайды презентации
Список похожих презентаций
Открытие нейтрона. Строение атомного ядра
Открытие нейтрона. Ирен Жолио-Кюри (1897-1956). Фредерик Жолио-Кюри (1900-1958). При бомбардировке бериллия α-частицами обнаруживалось какое-то сильно ...Строение атомного ядра и ядерные реакции
Модель атомного ядра. Изотопы некоторых химических элементов. «богатырь» с очень короткими руками. График зависимости энергии связи от атомного номера. ...Строение атомного ядра
Атом покорен, НО цивилизация под угрозой. Прав ли был Прометей, давший людям огонь? Мир рванулся вперед, мир сорвался с пружин, Из прекрасного лебедя ...Физика атомного ядра
Элементы содержания, проверяемые на ЕГЭ 2010: Радиоактивность. Альфа-, бета- и гамма-излучения Закон радиоактивного распада Нуклонная модель ядра ...Физика атома и атомного ядра
А -18. 1.На рисунке представлен фрагмент Периодической системы элементов Д. И. Менделеева. Под названием элемента приведены массовые числа его основных ...Физика атомного ядра и ее особенности
Радиоактивность - явление испускания атомами невидимых проникающих излучений Атомы радиоактивных веществ испускают три вида излучений различной физической ...Состав атомного ядра
ПЛАН УРОКА. 1.Протонно-нейтронная модель строения ядер. 2.Массовое число. 3.Зарядовое число. 4.Формула обозначения ядра. 5.Примеры. 6.Ядерные силы. ...Деление атомного ядра
. Деление ядра. . . . . ...Радиоактивность. Альфа-, бета-, гамма-распад атомного ядра
Цели: 1. Образовательные: познакомить с видами радиоактивного излучения; изучить виды радиоактивности; типами радиоактивного распада; 2. Развивающие: ...Строение кристаллов
Понятие кристаллов. Кристаллы – это твердые тела со строгим внутренним расположением атомов, которому соответствуют симметрия их внешних гладких поверхностей ...Строение вещества. Молекулы
Между частицами есть промежутки. При изменении температуры промежутки между частицами изменяются, при этом изменяется объем твердого тела. Промежутки ...Строение вещества, молекулы
Окружающие нас тела называются физическими телами. Всё то, из чего состоят физические тела, называют веществом. Из чего состоят вещества? Тема урока:. ...Строение вещества
Из чего состоит вещество? ? Твердые тела:. -при нагревание расширяются -при охлаждении сжимаются. Газы. При нагревание расширяются При охлаждении ...Строение вещества
Узнать из чего состоят вещества. Выяснить каковы размеры частиц вещества. Познакомиться с опытными доказательствами строения вещества. Цели урока:. ...Оболочечная модель ядра
При построении моделей ядра необходимо учитывать свойства сил, удерживающих протоны и нейтроны внутри ядра. Общей теории ядерных сил до сих пор не ...Строение атома
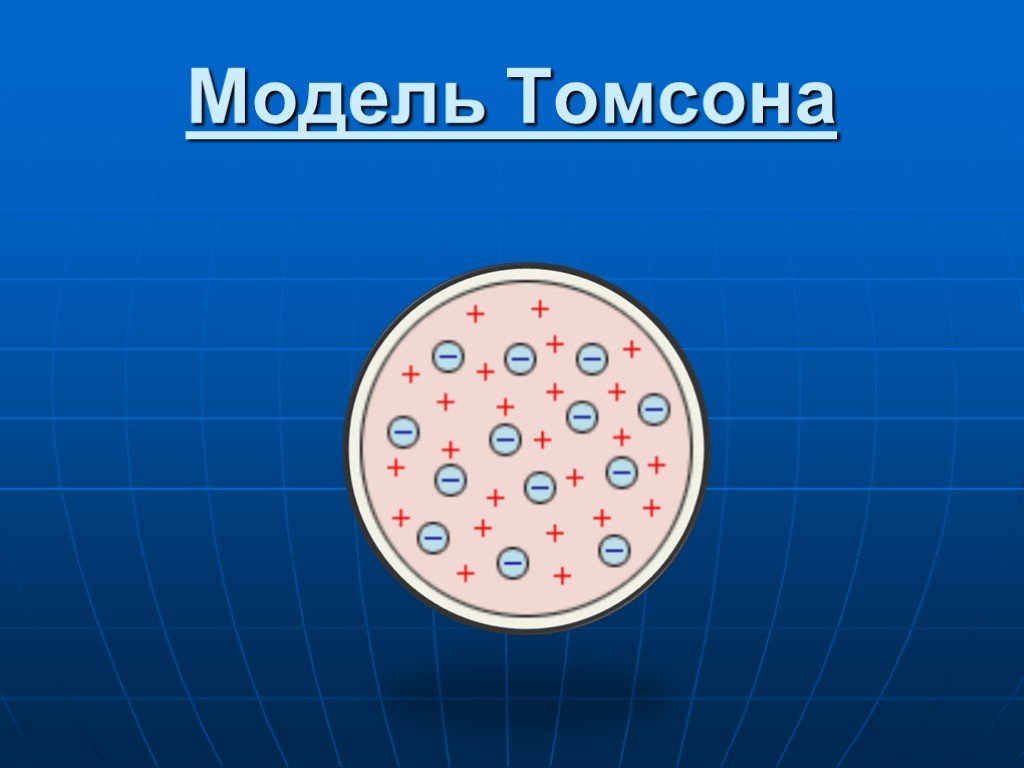
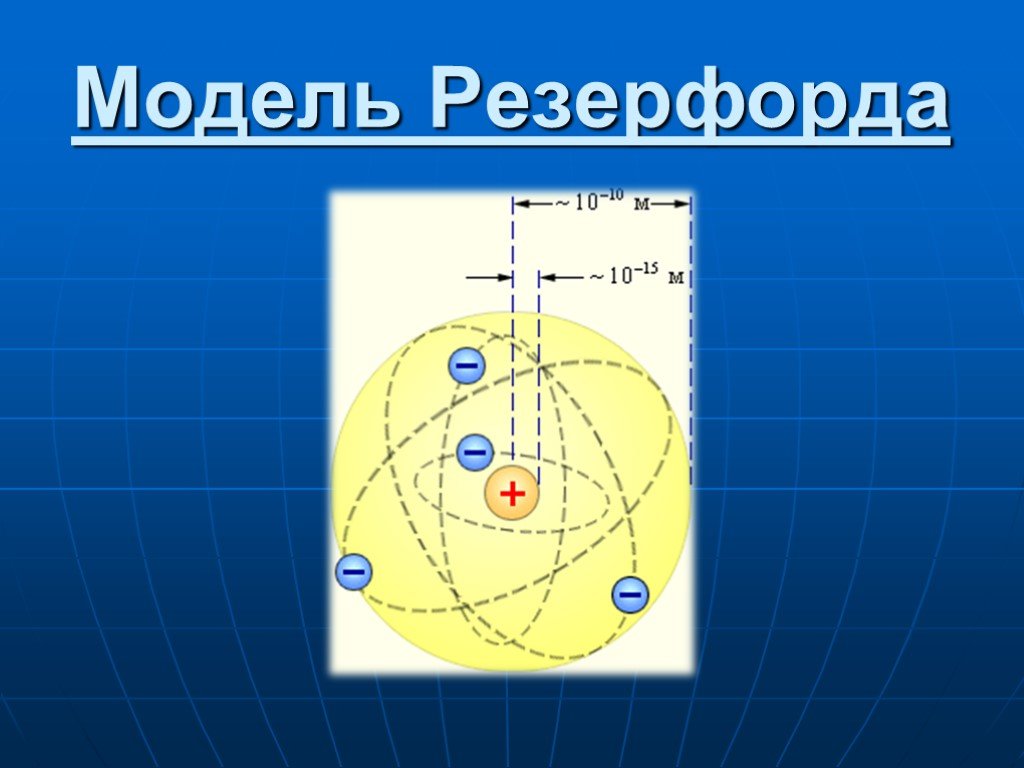
Английский физик Джозеф Джон Томсон (1856-1940). Лауреат Нобелевской Премии 1906 года. Английский физик Эрнст Резерфорд (1871 – 1937). Лауреат Нобелевской ...Состав ядра атома
План урока:. Вопросы для повторения. Изучение нового материала. Задачи и вопросы для закрепления пройденного материала. Вопросы для повторения. Что ...Радиоактивность . Строение атома
Левкипп Демокрит. Атом – «неделимый». 2500 лет назад. 1896 г. – открытие радиоактивного излучения «Лучи Беккереля». Анри Беккерель (1852-1908). Особые ...Анализ урока физики "Строение вещества. Молекулы".
Тип урока -. Комбинированный урок объяснения нового материала. Форма урока - Групповая. Тип группы - 4 – участника. Метод -. Исследовательский. Цели ...Конспекты
Радиоактивность. Строение атомного ядра. Радиоактивные превращения. Альфа-, бета-, гамма-распад: правило смещения. Закон радиоактивного распада и его статистический характер
Урок № 60-169 Урок № 60-169 Радиоактивность. Строение атомного ядра. . Радиоактивные превращения. Альфа-, бета-, гамма-распад: п. равило смещения. ...Строение атомного ядра
Урок физики в 9 классе. Тема: Строение атомного ядра. Цель урока:. познакомить учащихся с протонно-нейтронной моделью ядра, научить обобщать и ...Строение атома и атомного ядра
9 класс. . Урок № 8 в теме « Строение атома и атомного ядра». Ядерные силы, ядерные реакции. Энергия связи. Дефект масс. Цели урока : ...Состав атомного ядра. Массовое число. Зарядовое число. Изотопы
Тема: Состав атомного ядра. Массовое число. Зарядовое число. Изотопы. Тип урока: Объяснение нового материала. Цели урока:. . Образовательные. ...Путешествие в страну атомного ядра
. Разработка открытого урока по физике в 11А профильном физико – математическом классе. «Путешествие в страну атомного ядра». Урок подготовила. ...Повторение. Физика атомного ядра
Тема урока. : Повторение. Физика атомного ядра. Цель. : обобщение знаний об атоме, его строении, элементарных частицах, ученых, совершивший физические ...Открытие нейтрона. Состав атомного ядра. Массовое число. Изотопы
Нуриманов Д.Р., МКОУ СОШ №2. . Проект открытого урока. . «Открытие нейтрона. Состав атомного ядра. Массовое число. Изотопы». Цель:. Формирование ...Строение вещества
Урок физики в 7 классе. Строение вещества. Цель урока:. . Сформировать у обучающихся детальное представление о строении вещества. Ход урока. ...Строение вещества
Урок-исследование. Изучение нового материала. Строение вещества. 7-й класс. . Тип урока: комбинированный урок. Цели урока: сформировать представление ...Строение атомов
МБОУ СОШ №3 г. Навашино. Нижегородская область. УРОК ПО ФИЗИКЕ. . ТЕМА «Строение атомов». (8 класс, 13-14 лет). ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:2 мая 2019
Категория:Физика
Содержит:17 слайд(ов)
Поделись с друзьями:
Скачать презентацию