Слайд 1Синдром Марфана
Выполнила: студентка 4 гр. 3 мед. факультета Сыченко Д.Е. Преподаватель: Гречанина Ю.Б
Слайд 2Синдром Марфана (СМ), или Марфана-Ашара – это наследственное заболевание соединительной ткани с преимущественным поражением сердечно-сосудистой системы, скелета и органа зрения. Частота СМ в популяции составляет от 1:3000 до 1:15000. Впервые этот синдром описан французами – в 1896 г., педиатром Антонином Бернардом Марфаном, и в 1902 г. терапевтом Эмилем Шарлем Ашаром.
Слайд 3Существует интересный факт, что первая девушка модель - Лесли Хорнби, которая послужила прототипом образа всех моделей, имела синдром Марфана. Как, установлено, что ряд всемирно известных людей страдали синдромом Марфана, среди них следует упомянуть президента США А. Линкольна и великого скрипача Паганини.
Слайд 4Н. Паганини, Ш. де Голль, Г.Х. Андерсен, А. Линкольн.
Слайд 5Этиология и патогенез.
СМ относят к наследственным болезням соединительной ткани с аутосомно-доминантным типом наследования. Молекулярной основой заболевания является нарушение синтеза одного из белков соединительной ткани - фибриллина, который в норме придает ей эластичность и сократимость. При СМ вследствие дефицита фибриллина или его аномального строения соединительная ткань обладает повышенной растяжимостью и теряет способность выдерживать физиологические нагрузки. Ген фибриллина-1 располагается на длинном плече хромосомы 15, и картирован в локусе 15q21. Приблизительно в 75% случаев заболевание передается по наследству, остальные 25% вызываются спорадическими мутациями. Следует сказать, что СМ обладает выраженной генетической гетерогенностью.
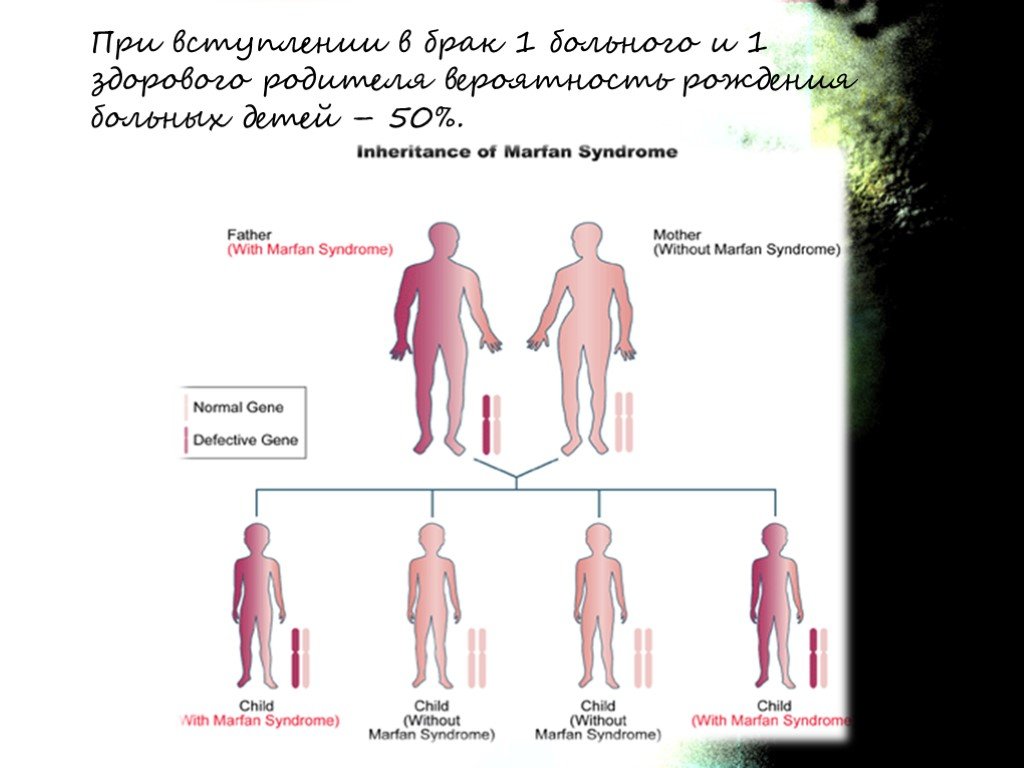
Слайд 6При вступлении в брак 1 больного и 1 здорового родителя вероятность рождения больных детей – 50%.
Слайд 7В настоящее время в различных семьях идентифицировано более 550 мутаций. Среди обнаруженных мутаций в гене FBN1 57% – миссенс мутации, 18% –фреймшифт (сдвиг рамки считывания), 16% – сплайс сайт, и 8% – нонсенс мутации. Чаще всего при классическом СМ имеет место мутация в одном из доменов FBN1 (epidermal growth factor (EGF)-like domain), ответственных за связывание кальция с фибриллином. Вследствие этого «незащищенный» кальцием фибриллин теряет устойчивость к протеазам, что приводит к дестабилизации микрофибрилл и нарушению их функции. Патологические изменения в одном и том же локусе могут обуславливать разнообразные клинические проявления – от стертой формы с поражением одной из систем организма до классической развернутой.

Слайд 8Классификация.
I. Форма: 1. Стертая: слабо выраженные изменения в одной, двух системах. 2. Выраженная: а) слабо выраженные изменения в трех системах. б) выраженные изменения хотя бы в одной системе (ограниченная форма). в) выраженные изменения в двух, трех системах и более. II. Характер течения: 1. Прогрессирующий. 2. Стабильный. III. Генетическая характеристика: 1. Семейная форма (тип наследования). 2. Первичная мутация.
Слайд 9IV. Клинические варианты: 1. Болезнь Марфана (присутствие трех классических признаков, семейный характер заболевания). 2. Синдром Марфана (наличие стертых форм с положительными нижеперечисленными диагностическими тестами). 3. Марфаноподобный синдром По МКБ-10 СМ относится к классу XVII: Врожденные аномалии [пороки развития], деформации и хромосомные нарушения; разделу Q87.: Другие уточненные синдромы врожденных аномалий [пороков развития], затрагивающих несколько систем и имеет код Q87.4.

Слайд 10Клиника.
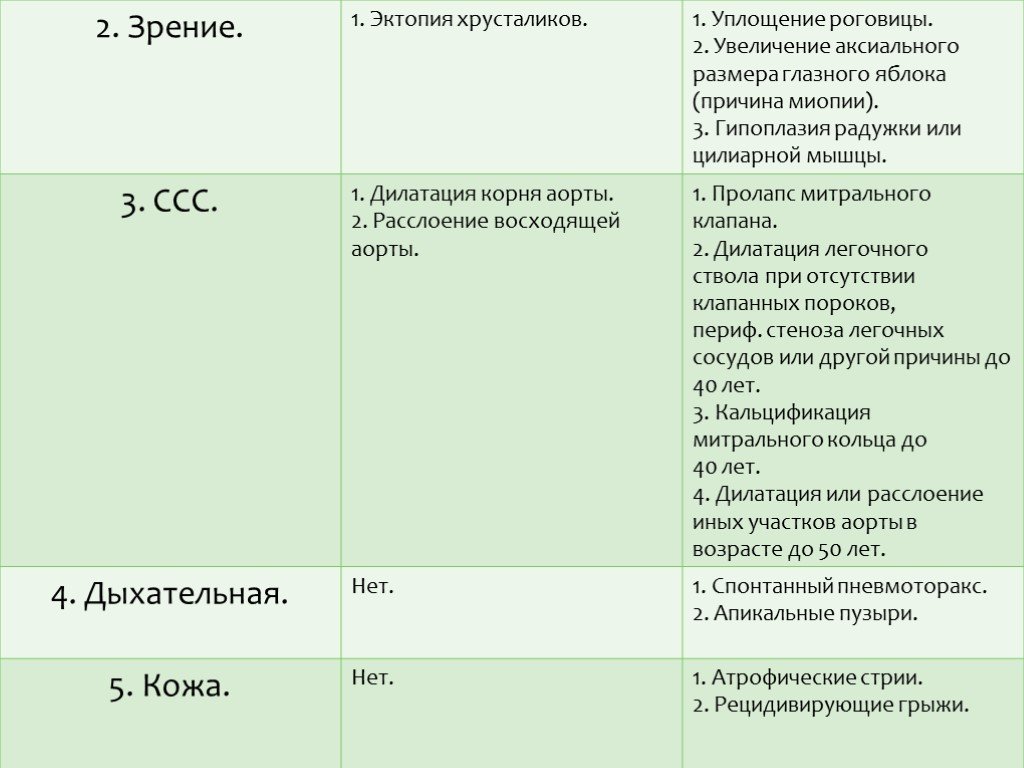
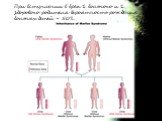
Поскольку фибриллин находится в соединительной ткани различных органов, симптоматика СМ многосистемна и разнообразна. При этом наиболее часто наблюдается сочетанное поражение сердечно-сосудистой системы, скелета и органа зрения. Естественно, тяжесть состояния и прогноз при СМ зависят, прежде всего, от степени поражения сердца и сосудов. Изменения сердечно-сосудистой системы отмечаются у большинства больных. Их основная причина – потеря способности стенок артерий и клапанных структур сердца выдерживать естественные гемодинамические нагрузки.

Слайд 11Наиболее частая сердечная патология при СМ – недостаточность митрального клапана. Обычно наблюдается поражение эластических структур створок и сухожильных нитей клапана с развитием его пролабирования и его недостаточности. Эта дисфункция митрального клапана рано или поздно у многих перерастает в умеренную или тяжелую митральную недостаточность, требующую хирургической коррекции. Реже бывает аортальная и трикуспидальная недостаточность. Стенозы клапанов для СМ не характерны. В связи с наличием у больных клапанных пороков, заболевание часто осложняется инфекционным эндокардитом.
ССС.

Слайд 12Патологические процессы со стороны аорты при СМ. Расширяется корень аорты, ее клапанное кольцо и синус Вальсальвы. Развивающаяся вследствие этого относительная аортальная недостаточность нередко приводит к кардиомегалии и тяжелой левожелудочковой недостаточности. Самым грозным осложнением является развитие расслаивающей аневризмы аорты с внутристеночной гематомой, проявляющееся выраженным болевым синдромом и тяжелыми гемодинамическими нарушениями, сто зачастую явлется причиной смерти больных СМ. Идентичные, но менее выраженные изменения могут быть и в легочной артерии. Так как при СМ сосудистая патология генерализованная, поражается эластическая ткань всех сосудов. Аневризмы могут возникать не только в различных отделах аорты, крупных ветвях легочной артерии, но и в венечных, сонных, лучевых, локтевых, бедренных, мозговых и других сосудах.

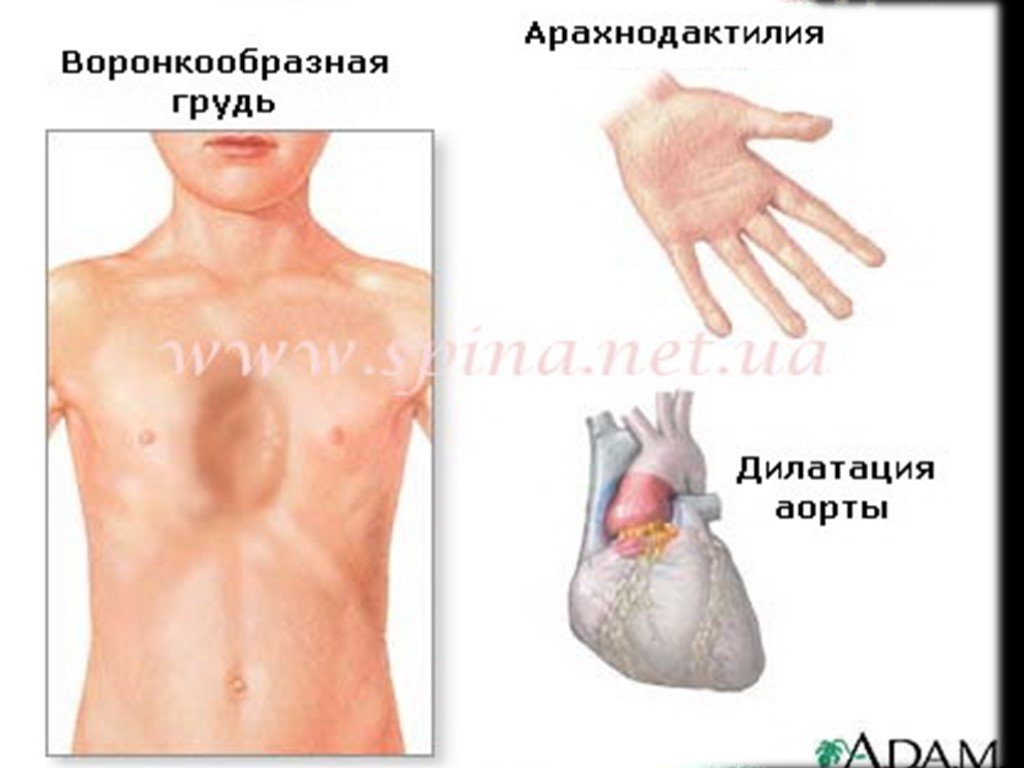
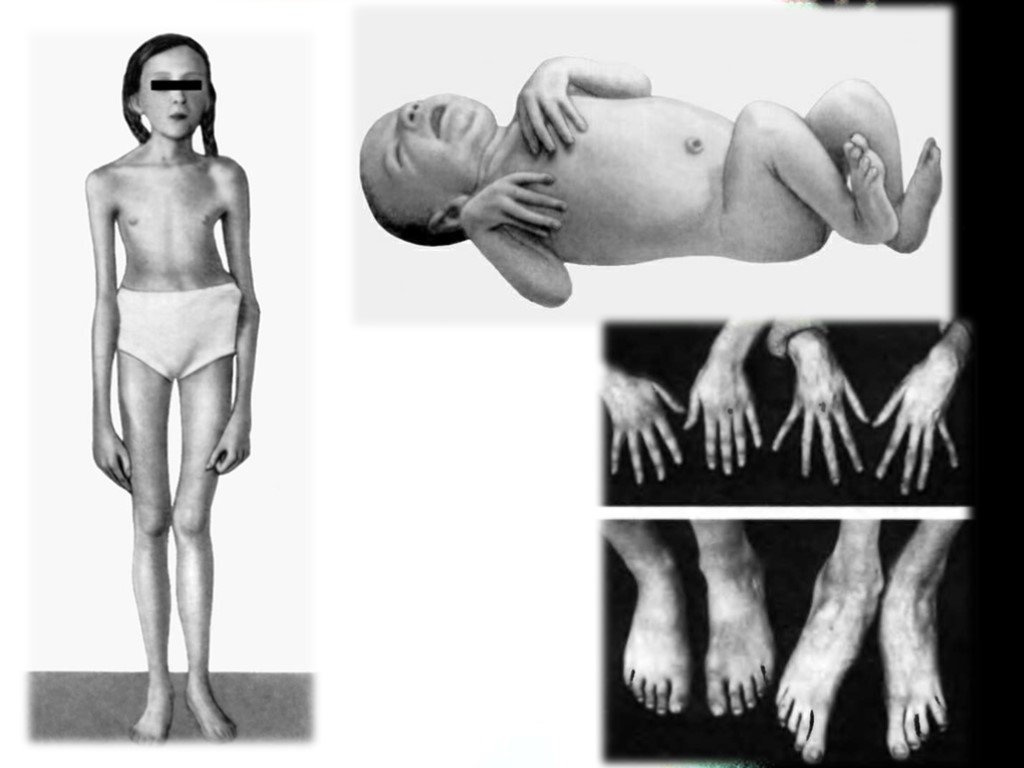
Слайд 13Проявления со стороны скелета наблюдаются у 2/3 пациентов. высокий рост, астеническое телосложение, долихостеномелию, долихоцефалию, прогнатию, "готическое" небо, деформация грудины («куриная» грудь или грудь «сапожника»), арахнодактилию, сколиозы и спондилолистезы, кифосколиозы, нарушение функции суставов, плоскостопие, протрузию вертлужной впадины, дисфункцию височно-нижнечелюстного сустава. Характерным является внешний вид больных: длинные и тонкие конечности с такими же пальцами, длинные, узкие ногти, «птичье лицо» (большой нос и маловыраженный подбородок).
Скелет.
Слайд 16Известны следующие фенотипические диагностические тесты СМ:
- соотношение кисть-рост > 11%; - отношение размаха рук к росту > 1,05; - длина среднего пальца > 10 см; - отношение длины верхнего сегмента тела к нижнему
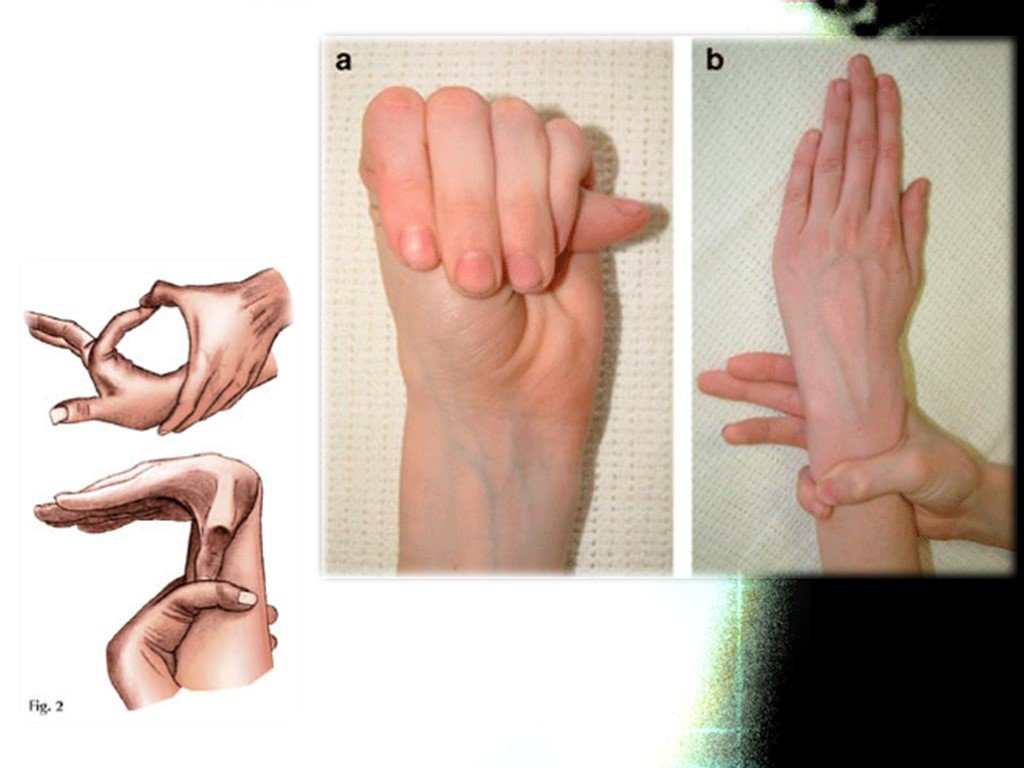
Слайд 17Весьма часто при СМ бывают положительными тесты на арахнодактилию:
а) тест большого пальца Steinberg: согнутый 1-й палец выступает за мягкие ткани кисти. При рентгенографии кисти с приведенным большим пальцем его фаланга выступает за скелет метакарпальных костей. б) тест запястья Walker-Murdoch: При обхватывании запястья другой. При арахнодактилии 1-й и 5-й пальцы соединяются друг с другом.

Слайд 19Офтальмологиеские признаки.
Наиболее часто встречается миопия различной степени, гипоплазия радужки, цилиарной мышцы и пигментной каймы зрачкового края, эктопия хрусталиков кверху, внутрь или кнаружи, реже – изменение калибра сосудов сетчатки, катаракта, зрачковая перепонка, косоглазие, дегенерация сетчатки, врожденная или вторичная глаукома. Эктопия хрусталиков вследствие надрывов, разрывов и деструкции связок постоянно прогрессирует, что отражается на зрительных функциях и плохо поддается коррекции очками. Наиболее часто эта патология хрусталиков встречается в среднем школьном возрасте, носит двусторонний характер, но степень ее выраженности может быть различной.

Слайд 20Нередко при СМ наблюдаются поражения со стороны других органов и систем:
Легких: поликистоз, эмфизема, спонтанный пневмоторакс); Желудочно-кишечного тракта: висцероптоз, недостаточность кардии; Почек (аплазия, поликистоз). Помимо этого, у больных СМ чаще, чем в общей популяции выявляют рецидивирующие паховые и бедренные грыжи, варикозное расширение вен, разрыв межпозвоночных связок, образования межпозвоночных грыж, опущение мочевого пузыря, матки, атрофические изменения кожи, эктазию твердой мозговой оболочки в пояснично-крестцовом отделе и т.д. Последний симптом считается одним из наиболее важных критериев диагностики заболевания.

Слайд 21Диагностика. Дополнительные методы исследования.
1. Лабораторные. Наиболее точным лабораторным признаком СМ является генетическая идентификация мутаций в гене FBN1. + показатели почечной экскреции метаболитов соединительной ткани: оксипролина, оксилизилгликозаминов, гликозаминогликанов и их фракционного состава (увел., как повышенный распад коллагена, а его уровень может определять тяжесть заболевания. 2. Электрокардиография. 3. Рентгенография. 4. Компьютерная томография. 5. Ангиография. 6. Эхокардиография. 7. Магнитно-резонансная томография (МРТ) 8. Генеалогический анализ.
Слайд 22Диагностические признаки синдрома Марфана.
Слайд 24Согласно «Гентской нозологии» для диагноза СМ необходимо, как минимум, наличие по одному большому критерию в двух системах и одного малого в третьей.
Слайд 25Лечение.
Консервативное. Так как ведущая причина смерти больных СМ - разрыв расслаивающей аневризмы аорты, то консервативное лечение направлено в первую очередь на его предотвращение. Еще в начале 70-х годов прошлого столетия было показано, что риск расслоения аорты у больных с СМ можно снизить путем длительного применения β-блокаторов (пропранолол, атенолол и метопролол). При наличии непереносимости или противопоказаний к применению β-блокаторов используют антагонисты кальция или ингибиторы ангиотензин превращающего фермента (АПФ). Стимуляция преждевременного полового созревания при помощи гормонотерапии может затормозить дальнейший рост и уменьшить проявления СМ у очень высоких детей.

Слайд 26Хирургическое. В настоящее время при СМ в основном применяется два типа вмешательств на аорте: комбинированная трансплантация по Bentall, при которой пересаживают корень аорты и ее клапан, 2. операции, сохраняющие аортальный клапан. 5-летняя и 10-летняя выживаемость при операции по Bentall - 80% и 60% соответственно, а операции с сохранением аортального клапана еще более эффективны: 5-летняя выживаемость превышает 90% .

Слайд 27Синдром Марфана и беременность.
Беременность при СМ опасна, по крайней мере, по двум причинам. 1. Имеется риск наследования заболевания, который составляет 50%. 2. Во время беременности и в раннем послеродовом периоде у больной женщины резко увеличивается риск расслаивающей аневризмы аорты и возникновения инфекционного эндокардита . Причина расслоения - увеличение ОЦК, аорто-кавальная компрессия и гормональные изменения. Риск этого осложнения возрастает пропорционально увеличению срока беременности. Роды через естественные родовые пути возможны у женщин, не имеющих выраженной патологии сердечно-сосудистой системы и диаметр аорты, не превышающий 4 см.

Слайд 28Диспансерное наблюдение.
В целях предотвращения прогрессирования заболевания и профилактики осложнений необходимо: 1. Регулярное наблюдение квалифицированных специалистов многопрофильной клиники. 2. Постоянный прием бета-адреноблокаторов (при отсутствии абсолютных противопоказаний). 3. Периодическое выполнение ЭхоКГ, МРТ или КТ для контроля диаметра аорты и клапанных пороков. 4. Профилактика инфекционного эндокардита в течение 6 месяцев после оперативного лечения, а также при имеющихся пороках клапанов.

Слайд 29Прогноз.
Продолжительность и качество жизни больных СМ в основном зависит от объема и выраженности поражения сердечно-сосудистой системы, скелета и глаз. Приемлемым для них является низкий или средний уровень физической активности. Из-за риска сердечно-сосудистых осложнений, развития пневмоторакса и возможной дислокации хрусталиков, им не рекомендуется заниматься контактными видами спорта и подводным плаванием. Оперированные пациенты имеют еще больше ограничений, особенно, если принимают антикоагулянты. Раннее начало лечения таких больных позволяет значительно увеличить продолжительность и улучшить качество их жизни. Без лечения средняя продолжительность жизни составляет 32+/-16 лет. При проведении полноценного лечения этот показатель увеличивается до 60 и более лет.
Слайд 30Спасибо за внимание!