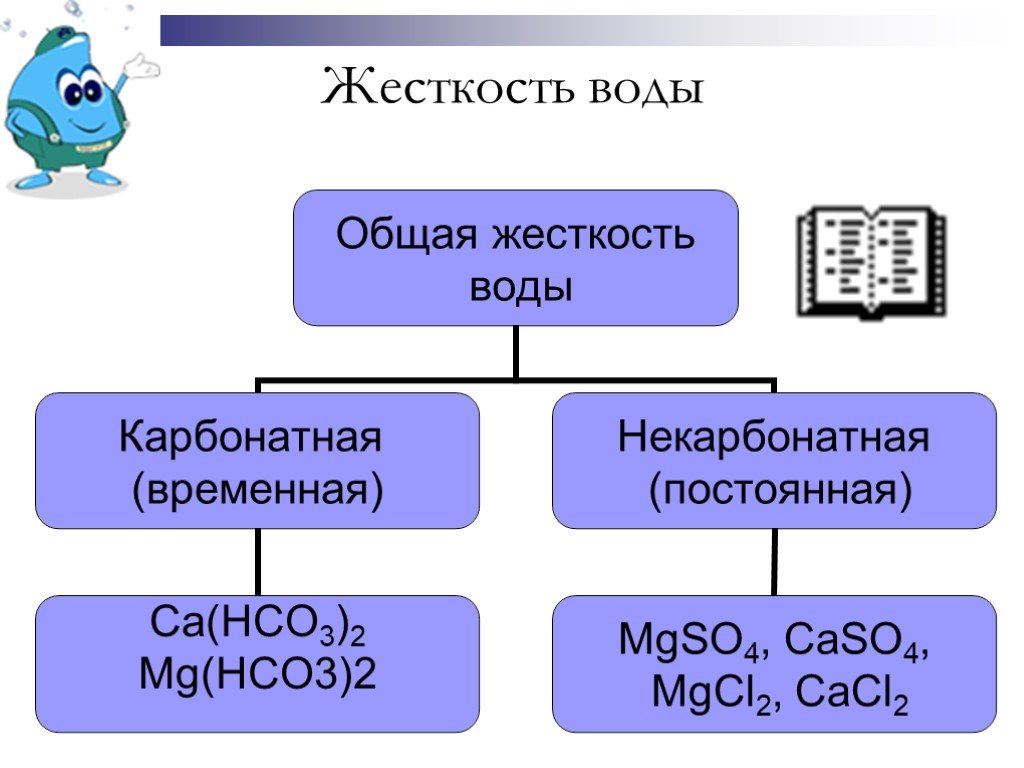
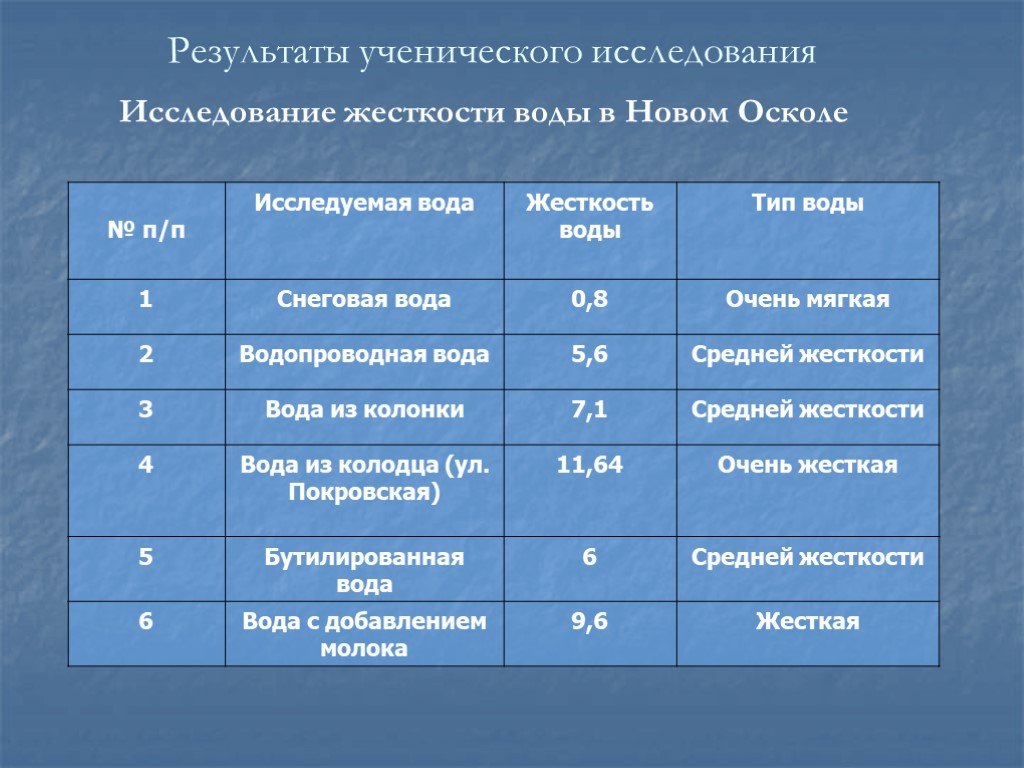
Презентация "Жесткость воды" по биологии – проект, доклад
Презентацию на тему "Жесткость воды" можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Биология. Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию. Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад - нажмите на соответствующий текст под плеером. Презентация содержит 13 слайд(ов).
Слайды презентации
Список похожих презентаций
Как защититься от загрязненной воды?
Главное для общества – не допускать загрязнение среды, охранять воду, воздух, почву. Решить эту задачу полностью пока не удается. Поэтому каждому ...Три состояния воды
Вы слыхали о воде? Говорят, она везде! В луже, в море, океане, И в водопроводном кране. Как сосулька, замерзает, В лес туманом заползает. Ледником ...Анализ родниковой воды
Вода – самое распространенное вещество на планете. Она занимает большую часть нашей планеты. Все живые организмы почти на 90 % состоят из воды. В ...Природные воды и оценка их качества
Это наш любимый город Сергиев Посад. Вода - химическое соединение водорода и кислорода - жидкость без запаха, вкуса, цвета. Вода уникальное вещество ...Роль воды в организме
Вода составляет около 60% от массы тела. В мышцах до 80%, в костях до 20%. В сутки в среднем потребляется 2,5 л: 1,2 л в виде жидкостей, 1 л с пищей, ...Нехватка питьевой воды
Запасы пресной воды находятся под угрозой из-за увеличения потребности в ней. Население растет и нуждается в ней все больше, а из-за изменений климата ...Влияние качества воды реки еруслан на здоровье
Цель работы: Изучить влияние качества воды реки Еруслан на здоровье школьников. Задачи: Изучить качество воды в реке Еруслан (приток Волги). Выявить ...Влияние разных источников воды на прорастание семян овса
Цель: Изучить влияние разных источников воды на прорастание семян овса. Задачи: Изучить литературу по происхождению, составу и свойствах воды; Дать ...Влияние живой и мёртвой воды на живые организмы
живая вода способствует лучшему росту растений, а мертвая вода их убивает. Цель работы:. изучить влияние живой и мёртвой воды на рост растений. Гипотеза:. ...Влияние качества воды на прорастание семян
Тема: Влияние качества воды на прорастание семян. Цель: Исследовать влияние качества воды на прорастание семян бобов. Задача: Поставить опыт и сделать ...Влияние живой и мёртвой воды на живые организмы
Как появилась вода…. Миллиарды лет назад в холодном газопылевом облаке, со временем сгустившемся, уплотнившемся и ставшем Землей, уже содержалась ...Влияние газированной воды на организм человека
Цель: исследование влияния газированной воды на организм человека. Задачи: найти информацию о влиянии газированной воды на здоровье человека; выяснить ...Биологическая роль воды
«Первое начало и сущность всего – вода» Фалес из Милета (VI в. до н.э.). Эта презентация проиллюстрирует Вам только некоторые сведения о том, какую ...Качество воды
Цель работы. Разработка метода эколого-водохозяйственной оценки состояния водных ресурсов бассейна речной системы, позволяющего: на основе обще доступных ...Всероссийский урок чистой воды
«Где вода, там и жизнь» и «Земля умирает, если ушла вода». Одна из причин сокращения запасов пресной воды – уменьшение водоносности рек, связанное ...Комплексная гигиеническая оценка колодезной воды из различных источников
И. Князев на приёме у Пахтановой А.В., главы администрации сельского поселения Рождественское. Вопрос дня: «Чистота водопроводной воды». 2. Актуальность ...Гигиена воды и водоснабжения населенных мест
Формы молекул воды. Молекулы воды могут существовать в следующих формах: 1) в виде одиночной молекулы воды – это моногидроль, или просто гидроль (Н2О)1; ...Круиз капли воды по миру
. . . . . . . . . . . Спасибо за внимание! ...День воды
Презентацию подготовила. учитель начальных классов МОУ лицей №7 г. Таганрога Ростовской области Великоднева Наталия Александровна. ...Конспекты
Свойства воды
. Муниципальное казённое специальное (коррекционное) образовательное учреждение для обучающихся, воспитанников с ограниченными возможностями здоровья ...Волшебная капелька воды
ГКС(К)ОУ «Специальная (коррекционная) общеобразовательная школа-интернат VIII вида с. Приволжское Ровенского района». Конспект открытого урока. ...Испарение воды растениями. Листопад
Разработка открытого урока по биологии в 6 классе. Учитель биологии Манченко Иван Сергеевич. Тема урока: «Испарение воды растениями. Листопад». ...Вода. Экологические проблемы использования воды
Муниципальное казенное общеобразовательное учреждение. «Нижнесанарская средняя общеобразовательная школа». Троицкого муниципального района Челябинской ...Советы как сделать хороший доклад презентации или проекта
- Постарайтесь вовлечь аудиторию в рассказ, настройте взаимодействие с аудиторией с помощью наводящих вопросов, игровой части, не бойтесь пошутить и искренне улыбнуться (где это уместно).
- Старайтесь объяснять слайд своими словами, добавлять дополнительные интересные факты, не нужно просто читать информацию со слайдов, ее аудитория может прочитать и сама.
- Не нужно перегружать слайды Вашего проекта текстовыми блоками, больше иллюстраций и минимум текста позволят лучше донести информацию и привлечь внимание. На слайде должна быть только ключевая информация, остальное лучше рассказать слушателям устно.
- Текст должен быть хорошо читаемым, иначе аудитория не сможет увидеть подаваемую информацию, будет сильно отвлекаться от рассказа, пытаясь хоть что-то разобрать, или вовсе утратит весь интерес. Для этого нужно правильно подобрать шрифт, учитывая, где и как будет происходить трансляция презентации, а также правильно подобрать сочетание фона и текста.
- Важно провести репетицию Вашего доклада, продумать, как Вы поздороваетесь с аудиторией, что скажете первым, как закончите презентацию. Все приходит с опытом.
- Правильно подберите наряд, т.к. одежда докладчика также играет большую роль в восприятии его выступления.
- Старайтесь говорить уверенно, плавно и связно.
- Старайтесь получить удовольствие от выступления, тогда Вы сможете быть более непринужденным и будете меньше волноваться.
Информация о презентации
Дата добавления:20 января 2019
Категория:Биология
Содержит:13 слайд(ов)
Поделись с друзьями:
Скачать презентацию