Слайд 1Энергетика химических процессов
Слайд 23. Определить степень превращения и условия равновесного состояния термодинамических систем.
химическая термодинамика позволяет
1. Определить тепловой эффект химических и физико-химических процессов.
2. Определить возможность и критерии самопроизвольного протекания физических и физико-химических процессов.
Слайд 3Основные понятия
Теплота – проявление кинетической энергии, связанное с движением атомов и молекул; Термодинамическая система (ТС) – отдельное тело или группа тел, состоящих из множества частиц, которые находятся во взаимодействии и обособлены от окружающей среды реальной или воображаемой оболочкой.
Открытая ТС Обменивается с окружающей средой теплотой и работой
Изолированная ТС Не происходит обмена с окружающей средой теплотой и работой
Слайд 4Параметры состояния: состав системы (характеризуемый одним или несколькими параметрами), температура, давление, объем. Функции состояния - функции, изменения которых зависит только от начального и конечного состояний системы и не зависит от пути перехода. Это U внутренняя энергия, H энтальпия, S энтропия, G энергия Гиббса Функции процесса – функции, зависящие от промежуточных значений. Это работа A, теплота Q
Слайд 5Если к системе подводится теплота Q, то в общем случае, она расходуется на изменение внутренней энергии ∆U и на совершение работы А
Q = ∆U + А
В любой изолированной системе запас энергии постоянен, т.е. внутренняя энергия является функцией состояния
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Слайд 6Внутренняя энергия U химической системы
Кинетическая составляющая – энергия движения на атомно-молекулярном уровне (движение молекул, колебания атомов, вращение электронов в атомах и т.д.) Потенциальная составляющая - энергия, заключенная в ядрах, энергия химических и межмолекулярных связей, энергия взаимного расположения атомов, ионов, молекул друг относительно друга в веществе, а также элементарных частиц в ядре.
Слайд 7Применение первого закона термодинамики Q = ∆U + А к различным процессам.
Изохорные процессы. V = const, ∆V = 0
А = р · ∆V
Т.к. ∆V = 0, то и А = 0. Тогда
QV - изохорный тепловой эффект реакции
QV = ∆U
Слайд 8Изобарные процессы. р =const, ∆р=0,
QР = U2 – U1 + р(V2 – V1); QР = U2 – U1 + рV2 – рV1
QР = (U2 + р·V2) – (U1 + р·V1)
Н- энтальпия
Н= U + р·V; QР = Н2 – Н1 = ∆Н
QР=∆U+р·∆V QР = ∆Н
QР - тепловой эффект изобарного процесса (P = const). называют изменением энтальпии системы или энтальпией процесса
Слайд 9Энтальпия H являетя энергетическим фактором и отражает изменение энергии взаимодействия между молекулами
*Изменение энтальпии ΔH характеризует тепловой эффект реакции: экзотермический процесс- выделение теплотыΔH 0
Стандартная теплота образования является характеристикой реакционной способности и устойчивости вещества: чем отрицательнее значение , тем более устойчиво вещество
энтальпия (Н= U + р·V)
Слайд 10Энтальпия образования простых веществ и катиона водорода в водном растворе принята равной нулю
Стандартная энтальпия образования
– тепловой эффект реакции образования одного моль вещества из простых веществ, взятых в устойчивых состояниях при стандартных условиях.
стандартные условия давление P = 101,325 кПа температура T = 298 K Концентрация С=1 моль\л
Слайд 11ТЕРМОХИМИЯ -
Тепловой эффект реакции -количество выделенного или поглощенного тепла при необратимом протекании хим.р-ции(Р илиV const),а единственной работой является работа расширения
Стандартные условия:
Р = 1атм( 101,3 кПа); Т=298 К (25 оC); n=1моль, С=1 моль/л
A= р·∆V
Слайд 12Термохимические (термодинамические) уравнения – уравнения химимческих реакций с указанием агрегатных состояний реагентов и теплового эффекта реакции
с термохимическими и термодинамическими уравнениями можно призводить любые алгебраические действия, т. е. складывать и вычитать их, умножать и делить на общий множитель, переписывать с соблюдением правила знаков и т.д. при условии, что термодинамические функции относятся к одинаковым условиям.
Н2 (г) + ½ О2(г) → Н2О (ж); ∆Н = - 286 кДж, ∆Н – термодинамический тепловой эффект
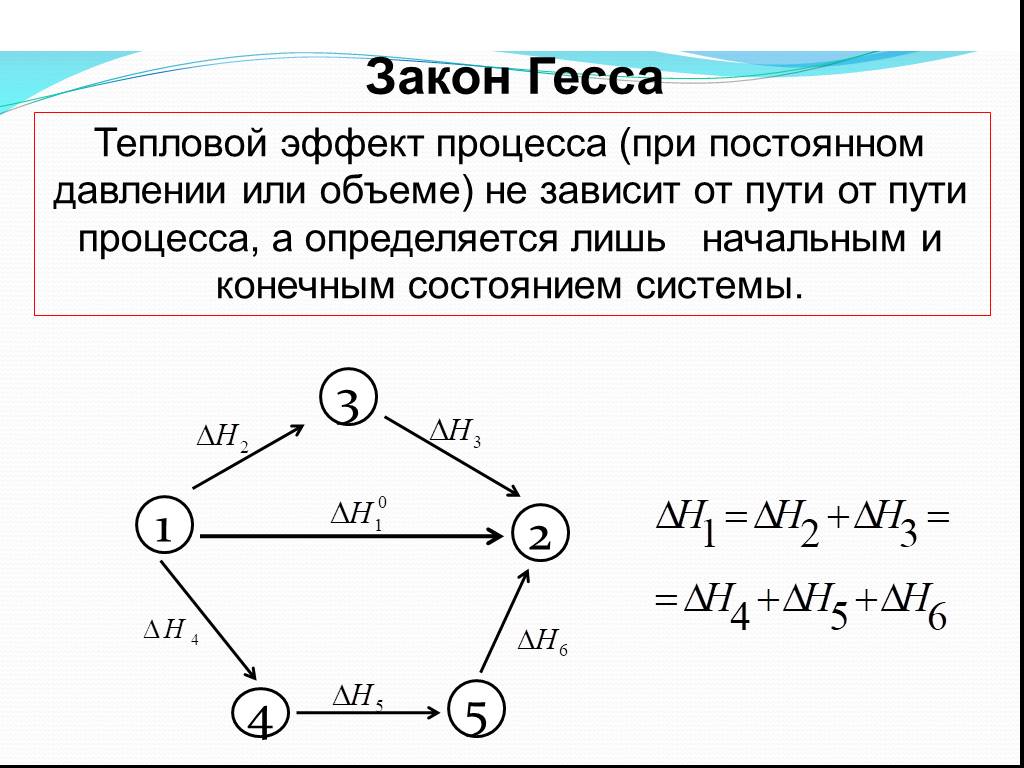
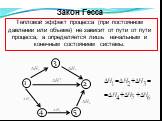
Слайд 13Тепловой эффект процесса (при постоянном давлении или объеме) не зависит от пути от пути процесса, а определяется лишь начальным и конечным состоянием системы.
Закон Гесса 1 3 2 4 5
Слайд 14Законы термохимии
Закон Лавуазье-Лапласса(1780 г.) Закон Гесса (1840 г.) Следствия из закона Гесса
В основе термохимических расчетов лежат
Закон Лавуазье-Лапласса
Энтальпия реакции образования вещества равна энтальпии реакции разложения его до исходных веществ с обратным знаком.
Слайд 15Тепловой эффект реакции равен разности сумм энтальпий образования продуктов и исходных веществ реакций с учетом их стехиометрических коэффициентов.
Следствия из закона Гесса
Расчет тепловых эффектов реакций электролитов необходимо производить для ионной формы реакции
Слайд 16Энтропия
Энтропия (S) – термодинамическая функция состояния, которая служит мерой беспорядка (неупорядоченности) системы
В изолированных системах энтропия самопроизвольно протекающего процесса увеличивается ΔS > 0
второй закон термодинамики
Слайд 17Термодинамическая вероятность W – число микросостояний, характеризующих данное макросостояние системы
Энтропия S [Дж/моль∙К] -
Энтропия идеального кристалла (W = 1) при абсолютном нуле равна нулю
постулат Планка
W- термодинамическая вероятность; S – энтропия; R = 8,31 Дж/моль∙К;
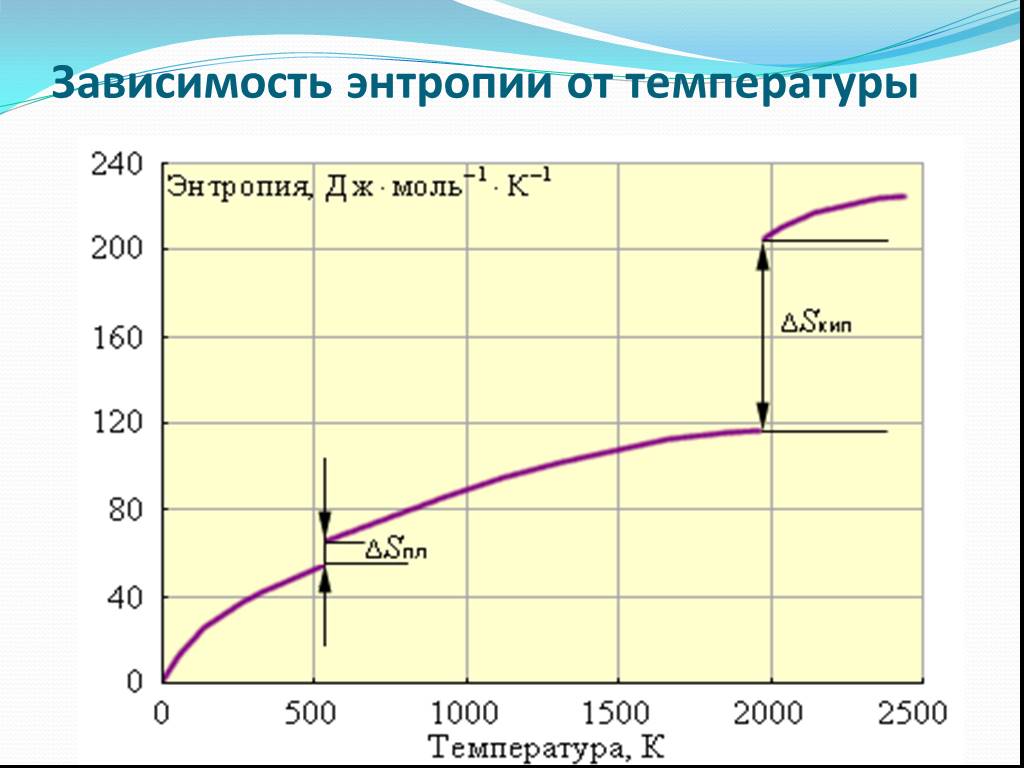
Слайд 18агрегатного состояния вещества. Энтропия увеличивается при переходе от твердого к жидкому и особенно к газообразному состоянию (вода, лед, пар). изотопного состава (H2O и D2O). молекулярной массы однотипных соединений (CH4, C2H6, н-C4H10). кристаллической структуры (аллотропии) – алмаз, графит.
энтропия зависит от
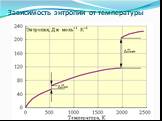
Слайд 19Зависимость энтропии от температуры
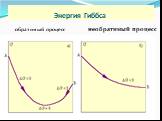
Слайд 20Энергия Гиббса ΔG реакция термодинамически разрешена ΔG = 0
равновесное состояние
ΔG > 0
термодинамически запрещен
процесс
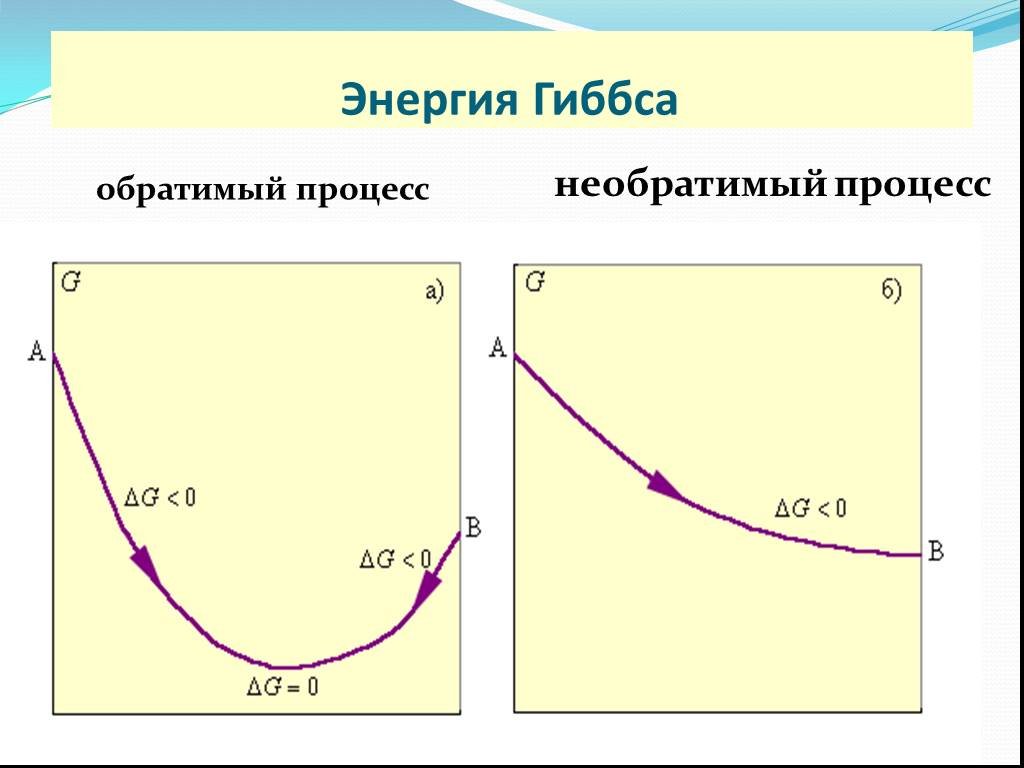
Знак ΔG определяет направление реального процесса
изобарно-изотермический потенциал или свободная энергия Гиббса (G, кДж/моль):
Слайд 21обратимый процесс
необратимый процесс
Слайд 22в химических процессах одновременно изменяются энергетический запас системы (энтальпийный фактор) и степень ее беспорядка (энтропийный фактор)
ΔH = ΔG + T ΔS
Энергия Гиббса, представляющая собой убыль изобарного (P = const) потенциала, равна максимальной полезной работе.
Уменьшаясь с течением химического процесса, ΔG достигает минимума в момент равновесия (ΔG = 0)
энтальпия реакции включает свободную энергию Гиббса и «несвободную» энергию ΔS · T.
энтропийный фактор T ΔS представляет ту часть энергии системы, которая при данной температуре не может быть превращена в работу. Эта связанная энергия способна лишь рассеиваться в окружающую среду в виде тепла (рост хаотичности системы).

Слайд 23Реакция возможна, если она сопровождается уменьшением изобарного потенциала; При комнатной температуре, когда значение T невелико, значение TΔS также невелико, и обычно изменение энтальпии больше TΔS.
Большинство реакций, протекающих при комнатной температуре самопроизвольно, экзотермичны.
ΔH Чем выше температура, тем больше TΔS, и даже эндотермические реакции становятся осуществимыми
В случаях , когда ΔH 0, ΔS > 0 знак ΔG зависит от соотношения ΔH и TΔS
Слайд 24Если ΔH 0, то всегда ΔG 0 и ΔS 0, и реакция с поглощением теплоты и уменьшением энтропии невозможна ни при каких условиях В остальных случаях (ΔH 0, ΔS > 0) знак ΔG зависит от соотношения ΔH и TΔS.
Слайд 25Стандартная энергия Гиббса образования вещества ΔG0обр.,298 (кДж/моль)
- это изменение энергии Гиббса реакции образования одного моля вещества из простых веществ в их устойчивой модификации и агрегатном состоянии при стандартных условиях. Если табличные значения ΔG0 обр, 298 0, то вещество неустойчиво и его нельзя получить напрямую из простых веществ, а можно получить только косвенным способом. Н2O (г) H2S(г) H2Se(г) ΔG0 обр, 298 - 228,45 -33,1 73,6 (устойчиво ) (не устойчиво)
Слайд 26условия некоторых возможных процессов
Слайд 27Расчет свободной энергии Гиббса (∆Gо) в химических реакциях
∆Gо298 обр. - стандартная из справочника
1) ∆Gореакции = ∑∆Gообр.продуктов - ∑∆Gообр.исх. в-в. с учетом стехиометрических коэффициентов.
2) ∆Gореакции = ∆Нореакции - T∆Sореакции
∆G
∆G>0, обратная реакция.
∆G=0, равновесие.
Слайд 28фазовые переходы и реакции термического разложнения
могут быть осуществлены
при









































![Термодинамическая вероятность W – число микросостояний, характеризующих данное макросостояние системы. Энтропия S [Дж/моль∙К] -. Энтропия идеального кристалла (W = 1) при абсолютном нуле равна нулю. постулат Планка. W- термодинамическая вероятность; S – энтропия; R = 8,31 Дж/моль∙К; Термодинамическая вероятность W – число микросостояний, характеризующих данное макросостояние системы. Энтропия S [Дж/моль∙К] -. Энтропия идеального кристалла (W = 1) при абсолютном нуле равна нулю. постулат Планка. W- термодинамическая вероятность; S – энтропия; R = 8,31 Дж/моль∙К;](https://prezentacii.org/upload/cloud/19/03/134949/images/thumbs/screen17.jpg)